





高中化学人教版 (新课标)选修4 化学反应原理第一章 化学反应与能量第三节 化学反应热的计算课堂教学ppt课件
展开1.能理解盖斯定律的本质,能说出其在科学研究中的意义。2.会运用盖斯定律进行有关反应热的简单计算。
一、盖斯定律1.内容不管化学反应是一步或分几步完成,其反应热是相同的。或者说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的 途径无关。2.解释能量的释放或吸收是以发生变化的物质为基础的,二者密不可分,但以物质为主。3.应用对于进行得很慢的反应,不容易直接发生的反应,产品不纯(即有副反应发生)的反应,测定这些反应的反应热有困难,如果应用 盖斯定律,就可以间接地把它们的反应热计算出来。
思考感悟同温同压下,氢气和氯气在光照条件下和点燃的条件下发生反应时的ΔH是否不同?提示:相同。化学反应的热效应与反应的始态和终态有关,与反应条件没有关系。
二、反应热的计算1.反应热计算的主要依据是热化学方程式、盖斯定律和燃烧热的数据。2.计算反应热的常用解题方法有列方程法、估算法、 十字交叉法等。
一、盖斯定律1.对盖斯定律的理解化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。若反应物A变为生成物D,可以有两个途径:①由A直接变成D,反应热为ΔH;②由A经过B变成C,再由C变成D,每步的反应热分别为ΔH1、ΔH2、ΔH3。如下图所示: 则有:ΔH=ΔH1+ΔH2+ΔH3
二、反应热的计算1.反应热的计算方法和类型(1)根据热化学方程式计算:反应热与反应中各物质的物质的量成比例。(2)根据反应物和生成物的能量计算:ΔH = 生成物的能量和-反应物的能量和。(3)根据反应物和生成物的键能计算:ΔH= 反应物的键能和-生成物的键能和。(4)根据盖斯定律计算:将热化学方程式进行适当的“加”“减”等变形后,由过程的热效应进行计算、比较。(5)根据物质燃烧放热数值计算:Q(放) = n(可燃物)×ΔH。(6)根据公式进行计算:Q=cmΔt。
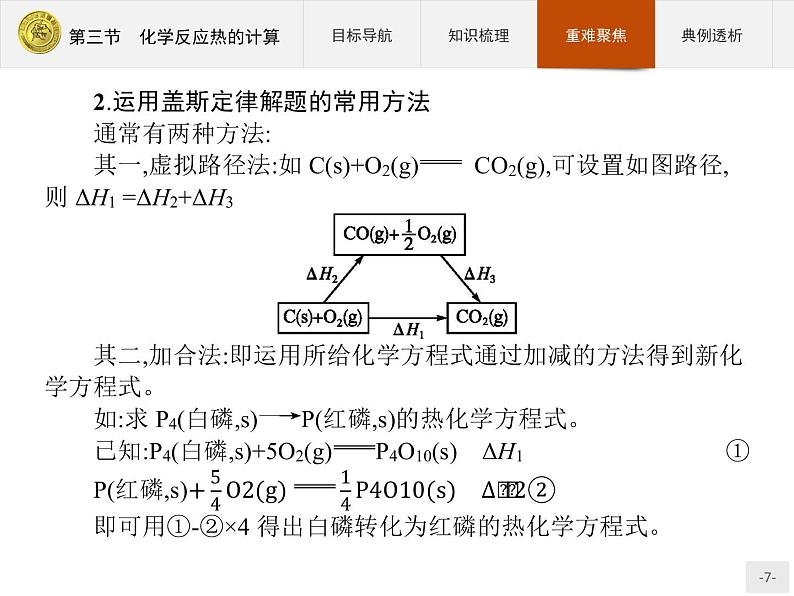
2.计算反应热的常用方法(1)列方程法:思路是先写出热化学方程式,再根据热化学方程式所呈现的物质与反应热间的关系直接求算反应热。(2)估算法:根据热化学方程式所表示反应的热效应与混合物燃烧放出热量,大致估算各成分的比例。此法主要应用于解答选择题,根据题给信息找出大致范围,便可以此为依据快速找出答案。(3)十字交叉法:混合物燃烧放热求比例问题,既可以采用常规的列方程组法,又可以采用十字交叉法。(4)将热化学方程式看作数学中的代数方程,扩大或缩小一定倍数后,直接加减或移项变形,得到需要的热化学方程式,再以此为依据求解或比较反应热大小等。
3.计算反应热应注意的问题(1)运用热化学方程式进行反应热的计算,可以利用反应式中各物质的物质的量、质量、标准状况下气体体积、反应热等对应关系,列式进行简单计算。(2)注意热化学方程式中化学计量数只表示物质的物质的量,必须与ΔH相对应,如果化学计量数加倍,则ΔH也要加倍。尤其是利用盖斯定律计算反应热时,热化学方程式可以直接相加减,化学计量数必须与ΔH相对应。(3)热化学方程式中的反应热是指按所给形式反应完全时的反应热。(4)正、逆反应的反应热数值相等,符号相反。
盖斯定律的应用【例题1】 室温下,将1 ml的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 ml的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2,CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是( )A.ΔH2>ΔH3 B.ΔH1<ΔH3C.ΔH1+ΔH3=ΔH2D.ΔH1+ΔH2>ΔH3
点拨应用盖斯定律进行简单计算,关键在于设计反应过程,同时要注意以下几点。(1)当热化学方程式乘以(或除以)某数时,ΔH也相应乘以(或除以)某数。(2)当热化学方程式进行加减运算时,ΔH也同样要进行加减运算,且要带“+”“-”符号,即把ΔH看作一个整体进行运算。(3)通过盖斯定律计算比较反应热的大小时,同样要把ΔH看作一个整体。(4)在设计的反应过程中常会遇到同一物质固、液、气三态的相互转化,物质的状态由“固→液→气”变化时,会吸热;反之会放热。(5)当设计的反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
A.-(0.4 ml×ΔH1+0.05 ml×ΔH3)B.-(0.4 ml×ΔH1+0.05 ml×ΔH2) C.-(0.4 ml×ΔH1+0.1 ml×ΔH3)D.-(0.4 ml×ΔH1+0.1 ml×ΔH2)
高中化学人教版 (新课标)选修4 化学反应原理第一章 化学反应与能量第三节 化学反应热的计算集体备课课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第一章 化学反应与能量第三节 化学反应热的计算集体备课课件ppt,共24页。PPT课件主要包含了目标导航,预习引导,问题导学,当堂检测等内容,欢迎下载使用。
化学选修4 化学反应原理第三节 化学反应热的计算背景图ppt课件: 这是一份化学选修4 化学反应原理第三节 化学反应热的计算背景图ppt课件,共58页。PPT课件主要包含了演示结束,分几步,ΔH2+ΔH3,直接发生,产品不纯,副反应发生,盖斯定律,热化学方程式,燃烧热,列方程式等内容,欢迎下载使用。
选修4 化学反应原理第三节 化学反应热的计算评课课件ppt: 这是一份选修4 化学反应原理第三节 化学反应热的计算评课课件ppt,共9页。













