




高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸优质课课件ppt
展开【学习目标】1、结合生活经验和观察乙酸样品,归纳乙酸的物理性质。2、观察模型,正确书写出乙酸的分子式、结构式和结构简式,并分析乙酸的结构特点。3.、回顾酸的通性,依据强酸制弱酸的原理设计实验比较醋酸与碳酸酸性的强弱。4.观察乙酸与乙醇反应的实验,简述操作步骤,描述实验现象;引导分析酯化反应的原理并能正确书写化学方程式。5.能举例说明乙酸在生活中的应用。
【学习重点】:官能团概念的理解,乙酸的分子组成及其化学性质【学习难点】:使学生建立立体结构模型,并能从结构角度初步认识乙酸的酯化原理。
传说古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”
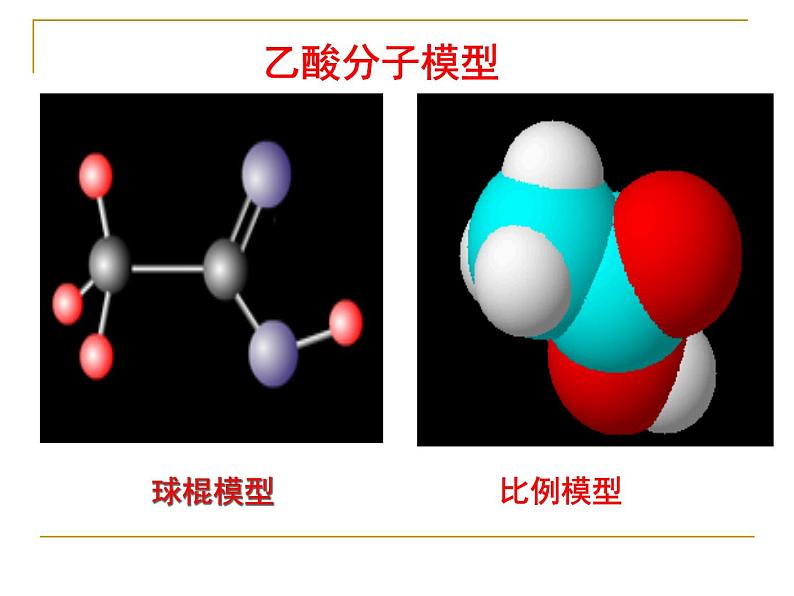
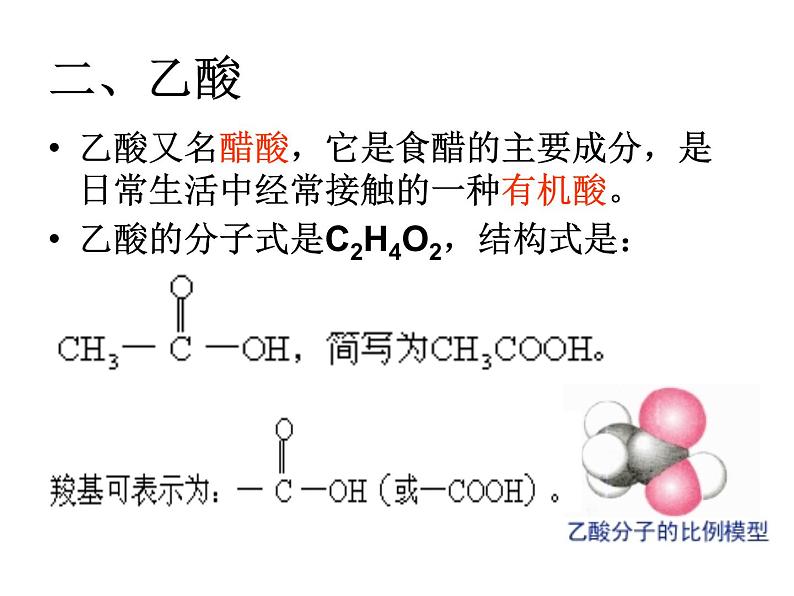
乙酸又名醋酸,它是食醋的主要成分,是日常生活中经常接触的一种有机酸。乙酸的分子式是C2H4O2,结构式是:
117.9℃ (易挥发)
(无水乙酸又称为:冰醋酸)
水垢主要成份:Mg(OH)2和CaCO3
2CH3COOH + CaCO3 = Ca(CH3COO)2 +H2O+CO2↑
判断酸性强弱顺序:
CH3COOH,H2CO3
酸性:CH3COOH>H2CO3
2CH3COOH + Na2CO3 = 2CH3COONa + CO2↑+ H2O
a、与Na2CO3溶液反应
Mg + 2CH3COOH → (CH3COO)2Mg + H2↑
离子方程式: 2CH3COOH + CO3 2- === 2CH3COO- +H2O+CO2↑
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
【学习目标】1、观察乙酸与乙醇反应的实验,简述操作步骤,描述实验现象;引导分析酯化反应的原理并能正确书写化学方程式。2、能举例说明乙酸在生活中的应用。
碎瓷片乙醇 3mL 浓硫酸 2mL乙酸 2mL饱和的Na2CO3溶液
(2)饱和Na2CO3溶液的作用?
①除去乙酸乙酯中混有的乙酸和乙醇②降低乙酸乙酯在水中的溶解度
乙酸乙酯的酯化过程 ——酯化反应的脱水方式
同位素原子示踪法判断酯化反应的本质。
【问题与讨论】酯化反应反应时,脱水可能有几种方式?
提示:如果用乙酸跟含18O的乙醇起反应,可发现生成物中乙酸乙酯分子中含有18O原子。
断键方式:酸脱羟基(-OH) 醇脱氢(H)酯化反应又属于取代反应。
探究酯化反应可能的脱水方式
定义:酸跟醇起作用,生成酯和水的反应实质:酸去羟基、醇去氢(羟基上的)注意:可逆反应
酯类广泛存在于自然界中
酯是有芳香气味的液体,存在于各种水果和花草中。如梨里含有乙酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。酯的密度一般小于水,并难溶于水,易溶于乙醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料和糖果的香料。
是一种重要的化工原料在日常生活中也有广泛的用途
3)乙酸的用途
【练习题】1、经常使用的修正液中往往含有某种易挥发的有毒 溶剂,应尽量减少或避免使用,这种溶剂可能是下列物质中的 ( )A、乙醇 B、 三氯乙烯 C、乙酸 D、水2、大理石可以用作墙面、地面和厨房桌面,其主要成份是碳酸钙、食醋不慎滴在大理石桌面上,会使其失去光泽,变得粗糙,下列能正确解释此现象的是A、食醋中的水使碳酸钙溶解 B.食醋中的醋酸将碳酸钙氧化C.食醋中的醋酸与碳酸钙反应并放出大量的二氧化碳气体D.食醋中的醋酸与碳酸钙发生了复分解反应
3.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是( ) A.金属钠 B.溴水 C.碳酸钠溶液 D.紫色石蕊试液
4.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( ) A.蒸馏 B.水洗后分液 C.用过量饱和碳酸钠溶液洗涤后分液 D.用过量氢氧化钠溶液洗涤后分液
5. 关于乙酸的下列说法中不正确的是 ( ).A.乙酸易溶于水和乙醇B.无水乙酸又称冰醋酸,它是纯净物C.乙酸是一种重要的有机酸,是有刺激 性气味的液体 D.乙酸分子里有四个氢原子,所以不是一元酸
6、 酯化反应属于( ).A.中和反应 B.不可逆反应C.离子反应 D.取代反应
7.用30g乙酸和46g乙醇反应,如果实际产率是理论产率的85%,则可得到的乙酸乙酯的质量是( )A.37.8g B.44g C.74.8g D.88g
58 46 86
30g 46g Xg
求得: X = 44.48g
实际产量 = 44.48g x 85% = 37.8g
沪科技版(2020)必修第二册乙酸试讲课课件ppt: 这是一份沪科技版(2020)必修第二册<a href="/hx/tb_c4036406_t3/?tag_id=26" target="_blank">乙酸试讲课课件ppt</a>,文件包含732乙酸备课件修复的pptx、732乙酸备作业原卷版docx、732乙酸备作业解析版docx、乙酸的性质实验酯化反应mp4、乙酸的性质-酸性与碳酸盐反应mp4等5份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
高中化学沪科技版(2020)必修第二册第7章 常见的有机化合物7.3 乙醇和乙酸乙酸课文课件ppt: 这是一份高中化学沪科技版(2020)必修第二册第7章 常见的有机化合物7.3 乙醇和乙酸乙酸课文课件ppt,共19页。PPT课件主要包含了结构简式,官能团,乙酸化学性质,2酸性比较,Na2CO3,饱和NaHCO3,Na2SiO3,醋酸盐酸,醇脱氢,酯水解反应-取代反应等内容,欢迎下载使用。
必修 第二册第三节 乙醇与乙酸一等奖课件ppt: 这是一份必修 第二册第三节 乙醇与乙酸一等奖课件ppt,共36页。PPT课件主要包含了学习目标,第2课时乙酸,乙酸的物理性质,乙酸的结构,乙酸的性质,与指示剂反应,与金属反应Zn,与碱作用NaOH,酸的通性,电离方程式等内容,欢迎下载使用。













