





化学必修1第二节 化学计量在实验中的应用课堂教学ppt课件
展开熟悉的知识
2H2+ O2 2H2O
4g 32g 36g
2个 1个 2个
一、物质的量的单位——摩尔
水是大家非常熟悉的物质,它是由水分子构成的,一滴水(约0.05 mL )大约含有1.7万亿亿个水分子。如果一个个地去数,即使分秒不停,一个人一生也无法完成这项工作。那么,则样才能既科学又方便地知道一定量的水中含有多少个水分子呢?
物质的量是把微观粒子和宏观物质联系起来的 一座桥梁。
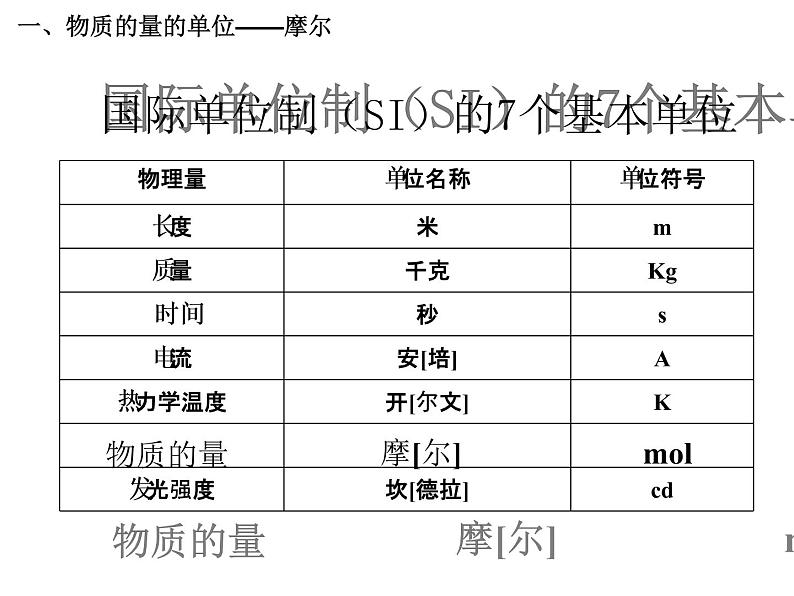
国际单位制(SI)的7个基本单位
物质的量的含义是什么?符号是什么?单位是什么?
是国际单位制七个基本物理量之一,符号为n 。
物质的量是表示含有一定数目微观粒子的集合体。
分子、原子、离子、电子、质子、原子团、中子等
单位 —— 摩尔 简称摩
使用物质的量注意事项:
①物质的量这四个字是一个整体,是一个专用名词,不得简化或增添任何字。
③物质的量计量的是粒子的集合体,不是单个粒子。
②物质的量只适用于微观粒子,使用摩作单位时,所指粒子必须指明粒子的种类,如原子、分子、离子等,且粒子的种类一般都要用化学符号表示。
判断正误,并说明理由。A.1 ml 氢B. 1ml CO2C. 1ml大米
错误。没有指出是分子、原子或离子
错误。大米不是微观粒子
必须指明粒子的种类,如原子、分子、离子等。
同0.012千克12C中所含的碳原子的数目相同 1摩尔
1 ml 任何粒子的集合体都含有约6.02×1023 个粒子。
一个碳原子的质量: 1.99×10-23克
所以,12克/ 1.99×10-23克≈6.02×1023
6.02×1023 ml-1叫做阿伏加德罗常数,它是个物理量,其是单位是ml-1,符号为NA 。
NA≈ 6.02×1023 ml-1
如果把6.02×1023个直径为2.5cm的硬币排成一行,可以来回于地球与太阳之间240.8亿次
如果把 6.02×1023 粒米给全球60亿人吃,每人每天吃一斤,要吃14万年,所以物质的量只用来表示原子、分子、离子等微观粒子。
(约6.02×1023ml-1)
物质的量( n ) 、粒子个数( N )和阿伏加德罗常数( NA )三者之间的关系:
物质的量(n)
变换为 N= n × NA
【规律】物质的粒子数之比 = 物质的量之比
在0.5 ml O2中含有的氧分子数目是多少?
N(O2)= n(O2) × NA
=0.5 ml× 6.02 ×1023ml-1
= 3.01 × 1023
答:O2的氧原子数为3.01 × 1023个。
先公式、后数字;标明每一个量的所属;带单位计算。
在0.5 ml O2中含有的氧原子数目是多少?
解:每个O2分子中含有两个氧原子,氧原子数为
N(O)= n(O2)×2 × NA
=0.5 ml×2× 6.02 ×1023ml-1
= 6.02 × 1023
答:O2的氧原子数为6.02 × 1023个。
1 、0.5 ml H2约含有氢分子数 个
2、 1 ml NaCl约含有氯离子数 个
3 、 1 ml 硫酸分子约含有氧原子数 个
4、 1. 2041024 个水分子物质的量为 ml
3.01 1023
6.02 1023
2.408 1024
5、2ml CO2中含有 ml C和 ml O, 含有 个CO2分子。6、 ml H2O中含有的氧原子数与1.5 ml CO2中含有的氧原子数相同。
1.204 1024
化学反应方程式中,系数之比即反应过程中各物质的物质的量之比
实验中,如何取出1ml或2ml粒子、或更多物质的量的物质
假如每颗米的质量都一样,现知道每10000颗米的质量都为5公斤.那么要取10000颗米时,你用数的还是用称的?
请找出1 ml 物质的质量有什么规律
定义:单位物质的量(即1ml)的物质所具有的质量叫做该物质的摩尔质量
单位:g · ml-1
结论: 1 ml 任何粒子或物质的质量以g为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。
物质的量( n ) 、质量( m )和摩尔质量( M )三者之间的关系:
变换为 m= n × M
例题、 71 g Na2SO4中含有的Na+和SO42-的物质的量多少?
2.等质量的下列物质中,所含分子数最少的是 ( )A、Cl2 B、 HCl C、NH3 D、H2SO4
3、1g H2O中含有a个氢原子,则阿伏加德罗常数为( )A、(a/9)ml-1 B、 9a ml-1 C、 2a ml-1 D、a ml-1
【练习】1.课本P13 学与问
人教版 (新课标)必修1第二节 化学计量在实验中的应用图片ppt课件: 这是一份人教版 (新课标)必修1第二节 化学计量在实验中的应用图片ppt课件,共26页。
高中人教版 (新课标)第二节 化学计量在实验中的应用教学演示ppt课件: 这是一份高中人教版 (新课标)第二节 化学计量在实验中的应用教学演示ppt课件,共33页。PPT课件主要包含了物质的量浓度,例题课本P15,容量瓶的规格,①配制步骤八字方针,称量产生误差,定容时俯视刻度,定容时仰视刻度,定容误差,误差分析,均无影响等内容,欢迎下载使用。
化学人教版 (新课标)第一节 物质的分类图文课件ppt: 这是一份化学人教版 (新课标)第一节 物质的分类图文课件ppt,共21页。PPT课件主要包含了金属单质,非金属单质,化合物,稀有气体,思考与交流1,氧化物,按是否含氧,按提供氢离子数目,按挥发性,按是否可溶于水等内容,欢迎下载使用。













