






化学第一节 无机非金属材料的主角--硅教课内容课件ppt
展开硅酸钠:水溶液叫水玻璃。
用水玻璃浸过的物品可以防火
肥皂填料、黏胶剂、阻燃剂
硅酸盐是由硅、氧和金属组成的化合物的总称,在自然界分布极广。硅酸盐是一类结构复杂的化合物,一般都不溶于水,化学性质很稳定。
几种硅酸盐产品——陶瓷、玻璃、水泥,最重要的无机非金属材料。
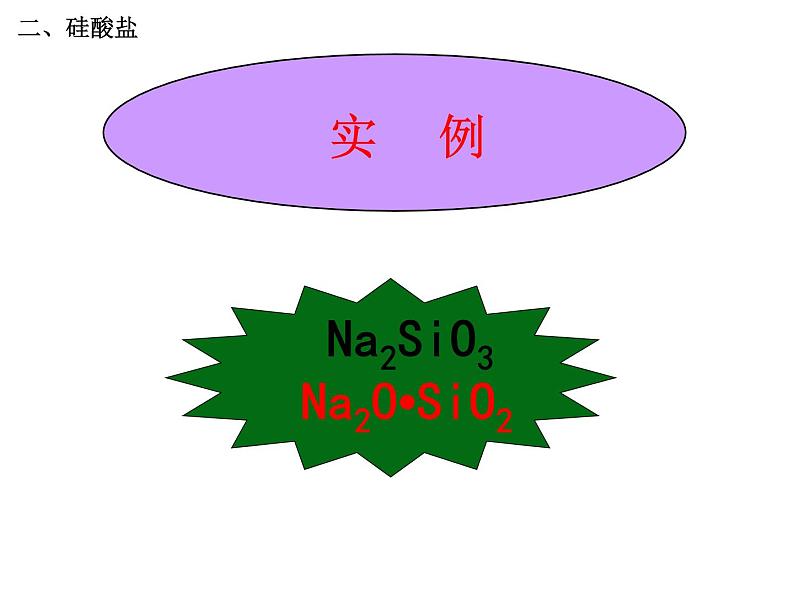
硅酸盐的一般特点:☆一般不溶于水(除Na、K盐外)化学稳定性高。☆种类繁多、结构复杂、构成地壳的骨架。☆通常用氧化物的形式表示其组成。如Na2SiO3 写成Na2O·SiO2
Al2(Si2O5)(OH)4
要领:两边原子个数守恒格式:金属氧化物、二氧化硅、水顺序:金属按活动性顺序表
K(Al3Si3O10)(OH)2
Na2SiO3 Na2O·SiO2CaSiO3 CaO·SiO2粘土:Al2O3·2SiO2·2H2O玻璃:Na2O·CaO·6SiO2水泥: 3CaO·SiO2; 2CaO·SiO2; 3CaO·Al2O3
自然界变化: 硅酸盐岩石→粘土→土壤胶体→吸收NH4+、K+等营养离子→供生物吸收。
水泥:以石灰石和黏土为原料
玻璃:以纯碱、石灰石和石英为原料 普通玻璃: Na2O·CaO·6SiO2
陶瓷(China):以粘土原料
SiC硅钢(4%)硅橡胶
硅有晶体硅和无定形硅两种单质
①灰黑色,有金属光泽,硬而 脆的固体②熔、沸点高、硬度大③晶体硅是良好的半导体
常温下,硅的化学性质不活泼,除氢氟酸、氟气、强碱外不跟其他物质如:氧气、氯气、硫酸等起反应,但在加热情况下,硅也能跟一些非金属反应。
(2)、与氢氟酸反应:
(3)、与强碱溶液反应:
Si+2F2==SiF4
Si+4HF==SiF4↑+2H2↑
Si+2NaOH+H2O==Na2SiO3+2H2↑
集成电路、晶体管、硅整流器等半导体材料,还可以制成太阳能电池、硅的合金可用来制造变压器铁芯等。
注:SiCl4沸点为57.6℃
SiO2+4HF=SiF4↑ +2H2O
2Si+2NaOH+H2O=Na2SiO3 +2H2↑
2NaOH+SiO2= Na2SiO3+H2O
Si+2F2=SiF4
Si+4HF=SiF4↑ +2H2 ↑
Si + F2Si + HFSi + NaOH
加热能与某些非金属单质反应(O2、Cl2)
已知硅与强碱氢氧化钠溶液反应的化学方程式为:
现把11.5g钠和4.2g硅同时投入100g水中,在标况下可收集到H2多少L?(提示:与Si反应的NaOH是过量的)
Na—1/2H223 1/2×22.411.5 X
Si—2H228 2×22.44.2 Y
Y=(4.2 ×2 ×22.4)/28=6.72(L)
VH2=5.6+6.72=12.32(L)
在实验室里,将细砂粉(SiO2)与镁粉混合加热,也可得到粗硅,反 应的化学方程式为这样得到的硅不纯净,往往含有过量的镁、氧化镁及硅化镁(Mg2Si)等,这些杂质可用盐酸除去,有关反应的化学方程式为
MgO+2HCl==MgCl2+H2O
Mg2Si+4HCl==2MgCl2+SiH4
高中化学鲁科版 (2019)必修 第一册第2章 元素与物质世界第1节 元素与物质分类集体备课ppt课件: 这是一份高中化学鲁科版 (2019)必修 第一册第2章 元素与物质世界第1节 元素与物质分类集体备课ppt课件,共33页。PPT课件主要包含了纯硅的制备,SiO2的用途,实验探究,硅酸盐等内容,欢迎下载使用。
高中化学第一轮总复习4.10无机非金属材料的主角—硅完美课件PPT: 这是一份高中化学第一轮总复习4.10无机非金属材料的主角—硅完美课件PPT,共60页。
人教版 (新课标)必修1第一节 无机非金属材料的主角--硅课堂教学课件ppt: 这是一份人教版 (新课标)必修1第一节 无机非金属材料的主角--硅课堂教学课件ppt,共43页。PPT课件主要包含了Al-773%,O-4860%,Si-2630%,硅元素,是结构上的不同,科学视野P74,合作讨论等内容,欢迎下载使用。













