






人教版 (新课标)必修1第一节 无机非金属材料的主角--硅课堂教学课件ppt
展开画出硅的原子结构示意图
分析: 既不易失电子,又不易得电子,主要形成四价的化合物。
与哪种原子的结构相似?
常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?
单质硅的化学性质虽然稳定,但硅是一种亲氧元素,硅原子和氧原子的结合非常牢固,形成的二氧化硅或硅酸盐中的硅氧化学键非常牢固,硅氧键一旦形成就很难被破坏,所以,自然界中硅都是以二氧化硅或硅酸盐的形式存在,没有游离态的硅。
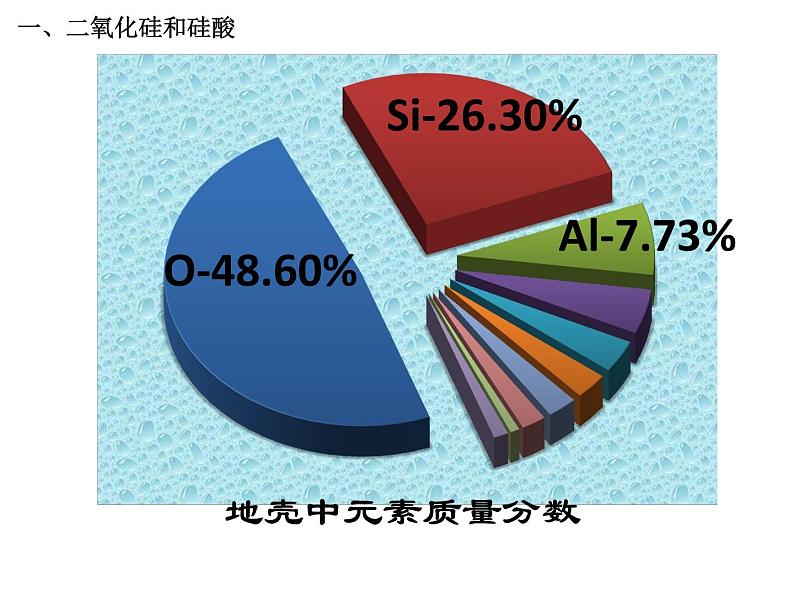
硅是一种亲氧元素,在自然界中主要以氧化物及硅酸盐的形式存在。
光导纤维石英:耐高温化学仪器、石英电子表、石英钟水晶:电子工业的重要部件、光学仪器、 高级工艺品和眼镜片玛瑙:精密仪器轴承、耐磨器皿和装饰品
物理性质:_____________________________
化学稳定性:_________________________
硬度大、熔点高、难溶于水
为什么二氧化硅和二氧化碳物理性质有这么大的差别?
实验室中盛放碱液的试剂瓶与盛放其 它溶液的试剂瓶有何不同?为什么 ?
1. 玻璃中含有SiO2,从物质组成和性质角度来分类, SiO2属于哪类物质?
2. SiO2可能具有哪些化学性质?
(a)常温与氢氟酸(SiO2很不活泼,HF是唯一能跟其反应的酸)
4HF+SiO2==SiF4↑+2H2O
(b)酸性氧化物:不溶于水,也不与水反应。
2NaOH+SiO2==Na2SiO3+H2O
(所以,不能用磨口玻璃塞盛碱性溶液,如NaOH、KOH、Na2CO3、Na2SiO3等溶液。)
HF能腐蚀玻璃,因此,盛装氢氟酸不能用玻璃试剂瓶而要用塑料瓶。
SiO2与CO2化学性质的比较
CO2+H2O=H2CO3
CO2+2NaOH=Na2CO3+H2O
CO2+Na2O=Na2CO3
SiO2+4HF=SiF4 ↑+2H2O
SiO2+2NaOH=Na2SiO3+H2O
SiO2+ CaO == CaSiO3
2.硅酸(H2SiO3)
硅酸是一种白色粉末状的固体,它不溶于水;是一种弱酸,不能使指示剂变色。
二氧化硅难溶于水,又不与水反应,那么,如何制得硅酸呢?
由可溶性硅酸盐与其他酸反应制备。
实验4-1:向饱和Na2SiO3溶液中滴入酚酞,再滴入稀盐酸
① Na2SiO3溶液呈碱性
Na2SiO3+2HCl = H2SiO3(胶体) +2NaCl
把稀硫酸加入到Na2SiO3溶液中,会有什么现象?
Na2SiO3+H2SO4 = H2SiO3 (胶体) +Na2SO4
所生成的硅酸逐渐聚合而形成胶体-硅酸溶胶,硅酸浓度较大时,则形成软而透明的、胶冻状的硅酸凝胶。硅酸凝胶经干燥脱水就形成硅酸干胶,称为“硅胶”。硅胶多孔,吸附水分能力强,常用做实验室和袋装食品、瓶装药品等的干燥剂,也可以用作催化剂的载体。
2、硅酸(H2SiO3)
Na2SiO3+2HCl=2NaCl+H2SiO3↓
② 弱酸性(酸性 H2SiO3 < H2CO3)
Na2SiO3+CO2+H2O=H2SiO3 (胶体) +Na2CO3
硅酸是一种比碳酸还要弱的酸。请利用中学实验室常见的仪器及药品,设计一个简单实验,证明硅酸的酸性比碳酸弱,并完成一份实验报告。
CO2通入下列各溶液中,无明显现象发生的是( )A、氯化钙溶液 B、澄清石灰水C、硅酸钠溶液D、饱和碳酸钠溶液
试剂二氧化硅氢氧化钠溶液氢氟酸浓硫酸
试剂瓶细口瓶,磨口塞广口瓶细口塑料瓶细口瓶,橡皮塞
1、实验室有几种试剂,根据它们各自的性质,选择适当的试剂瓶盛放。请在对应的各种试剂瓶和所装试剂之间进行连线。
2、下列说法正确的是( )A.SiO2溶于水显酸性B.CO2通入水玻璃(硅酸钠的水溶液)可得硅酸C.SiO2是酸性氧化物,它不溶于任何酸D.SiO2晶体中不存在单个SiO2分子
3、玻璃的主要成分之一是二氧化硅,能在玻璃上进行蚀刻,将其制成毛玻璃和雕花玻璃的物质是 ( ) A、烧碱 B、纯碱 C、氢氟酸 D、盐酸
高中化学鲁科版 (2019)必修 第一册第2章 元素与物质世界第1节 元素与物质分类集体备课ppt课件: 这是一份高中化学鲁科版 (2019)必修 第一册第2章 元素与物质世界第1节 元素与物质分类集体备课ppt课件,共33页。PPT课件主要包含了纯硅的制备,SiO2的用途,实验探究,硅酸盐等内容,欢迎下载使用。
化学第一节 无机非金属材料的主角--硅教课内容课件ppt: 这是一份化学第一节 无机非金属材料的主角--硅教课内容课件ppt,共24页。PPT课件主要包含了高岭石,拆分原则,硅酸盐产品,其它重要硅化物,科学视野新型陶瓷,不反应等内容,欢迎下载使用。
化学必修1第四章 非金属及其化合物第一节 无机非金属材料的主角--硅教课内容ppt课件: 这是一份化学必修1第四章 非金属及其化合物第一节 无机非金属材料的主角--硅教课内容ppt课件,共33页。













