








化学九年级下册课题2 溶解度课文内容ppt课件
展开【重点】理解溶解度的含义,利用溶解度曲线获得相关信息。
【难点】形成溶解度的概念。
1.理解溶解度的含义,初步学会绘制和分析溶解度曲线。2.知道影响溶解度的因素,能利用气体溶解度解释生活中的有关现象。
冬天捞碱 夏天晒盐
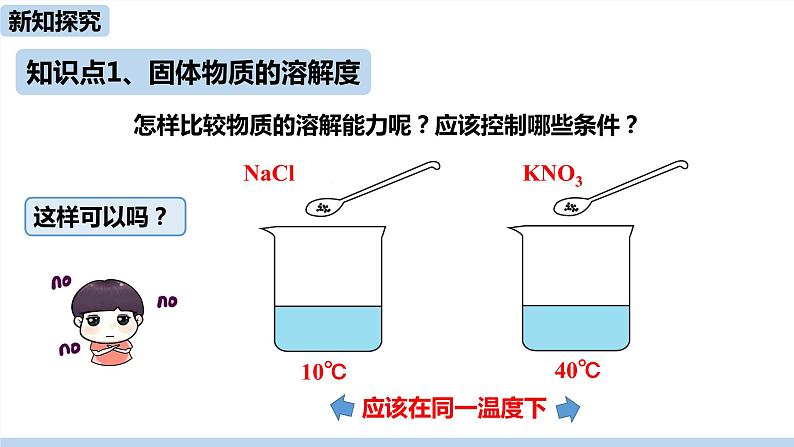
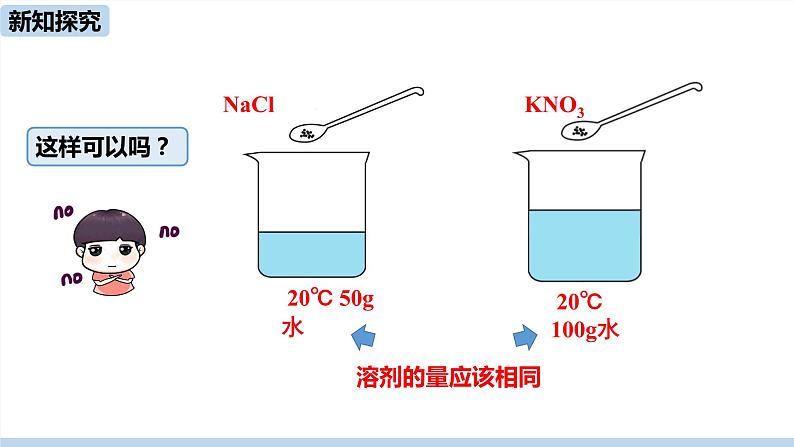
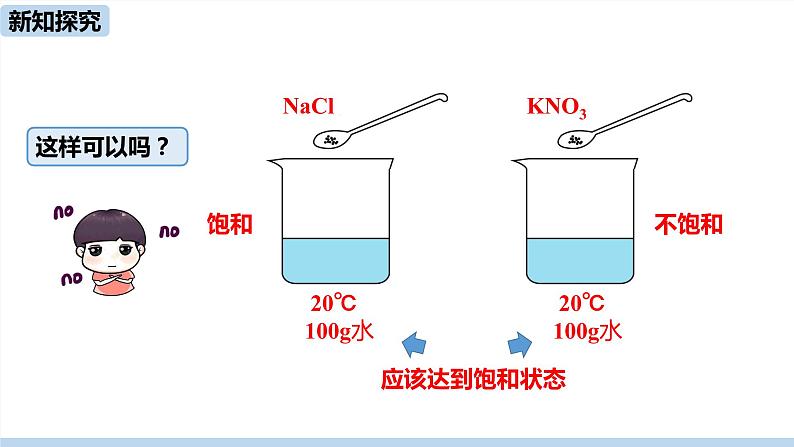
怎样比较物质的溶解能力呢?应该控制哪些条件?
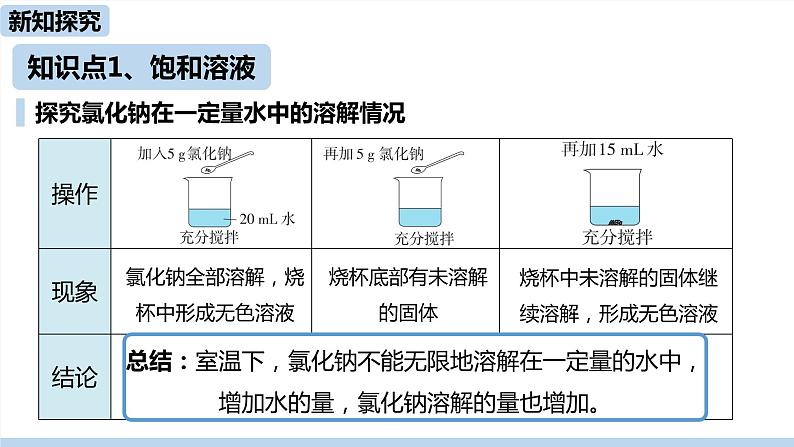
知识点1、固体物质的溶解度
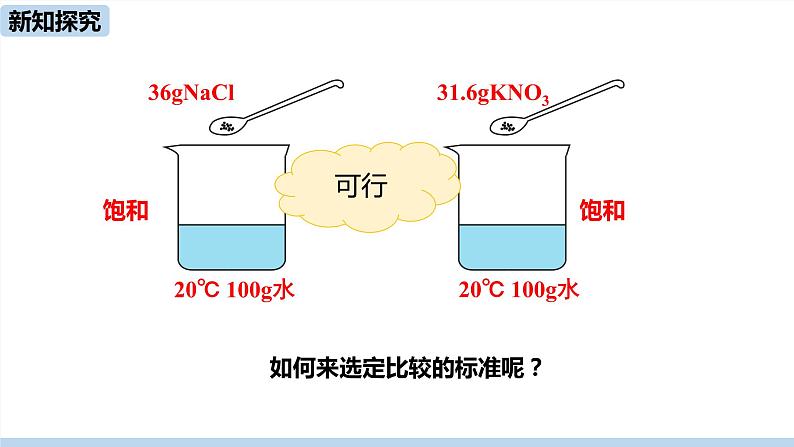
如何来选定比较的标准呢?
溶解度(s):在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
100g溶剂(一般指水)
固体物质溶解度的四要素
物质的溶解度会随温度的变化而变化,不指明温度时,溶解度没有意义
这是概念中规定的标准,物质溶解量的多少与溶剂量的多少成正比,要比较物质溶解度的大小,必须要设定等量的溶剂。
只有在一定量(100g)溶剂中,溶液达到饱和状态(溶解溶质的量最大)时,所溶解的溶质的量才是一个确定的值,这个值能够代表该物质在确定温度下,溶解能力的强弱。
溶解度实质上是100g溶剂中溶解溶质的最大质量
1.“20℃时,氯化钠固体的溶解度为36g”,其含义是什么?
在20℃时,100g水中溶解36g氯化钠固体,溶液达到饱和。
在20℃时,100g水中最多可溶解36g氯化钠固体。
2. “20℃时硝酸钾的溶解度是31.6g”,这句话的含义是什么?将其关系代入下表:
影响固体物质溶解度的因素
1.内因:溶质、溶剂本身的性质(或溶质和溶剂的种类)2.外因:温度。固体物质溶解度与溶剂量的多少没有关系,因为概念中溶剂的量已经规定为100g,所以在外部因素中固体物质溶解度只与温度有关。
固体物质溶解度与溶解性的关系
溶解性只是定性地说明某种物质在某种溶剂里溶解能力的大小,而溶解度是衡量某种物质在某种溶剂里溶解性大小的尺度。
(2019·成都模拟)20 ℃时,食盐的溶解度是36g,它的含义是( )
A. 20 ℃时,136g饱和食盐水中含有36g食盐B. 在100g水中最多溶解36g食盐C. 20 ℃时,饱和食盐水中含有36g食盐D. 20 ℃时,100g饱和食盐水中含有36g食盐
解析:溶解度的四要素:一定温度(20 ℃),100g溶剂(100g水), 饱和状态(最多能溶解氯化钠的量为36g),单位是克。
知识点2、固体物质溶解度的表示方法及其应用
用横坐标表示温度,纵坐标表示溶解度,根据实验测得的某物质在不同温度下的溶解度数据,在直角坐标系上描点并用平滑的曲线连接起来,即可绘制出溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
a.陡升型。大多数固体物质的溶解度随温度的升高而增大,表现为曲线坡度陡增,如KNO3、NH4NO3等。
b.缓升型。少数固体物质的溶解度受温度变化的影响较小,表现为曲线坡度比较平缓,如NaCl。
c.下降型。极少数固体物质的溶解度随温度的升高而减小,表现为曲线坡度下降,如Ca(OH)2。
1.查出某种物质在某温度时的溶解度。2.可以看出物质的溶解度随温度变化的规律。3.比较不同物质在同一温度时的溶解度大小。4.可以比较不同物质的溶解度受温度变化影响的大小。5.根据物质的溶解度曲线确定如何制得某温度时该物质的饱和溶液。6.确定混合物的分离、提纯方法。
如图,已知曲线a,b分别为两种固体物质甲、乙的溶解度曲线。
曲线a:物质甲的溶解度随温度的升高而增大,受温度变化影响较大。曲线b:物质乙的溶解度随温度的升高而缓慢增大,受温度变化影响较小。N点:物质甲在t1℃时的溶解度为S1g。P点:物质乙在t3℃时的溶解度为S3g。M点:在t2℃时物质甲和物质乙的溶解度相等,都为S2g。
当甲中含有少量乙(如KNO3中含有少量的NaCl)时,可采用冷却热饱和溶液(降温结晶)法分离(或提纯)出物质甲。当乙中含有少量甲(如NaCl中含有少量的KNO3)时,可采用蒸发结晶法分离(或提纯)出物质乙。
(2019·咸宁中考)如图为甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
A.甲中混有少量乙,若要提纯甲,可采取冷却热饱和溶液结晶法B.t2℃时,丙的饱和溶液中溶质和溶剂的质量比为1:4C.将t3℃的甲、乙饱和溶液降温到t1℃,析出固体甲的质量一定大于乙D.在t3℃时,甲、乙两物质的溶解度相等
1.概念:气体的溶解度是指该气体的压强为101kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。
2.气体溶解度概念中的四要素:(1)条件:在压强为101kPa、一定温度时。(2)标准:1体积水。(3)状态:达到饱和状态。(4)单位:体积。
在压强不变的条件下,温度越高,气体的溶解度越小
在温度不变的条件下,压强越大,气体的溶解度越大
气体溶解度与固体溶解度的比较
(2019·山东东营中考)夏季,鱼虾养殖池内常设置一些水泵,把水喷向空中,从化学角度分析,喷水的目的是( )
A.降低养殖池内水的温度B.增大与空气的接触面积,便于氧气溶解C.增加观赏性D.便于太阳照射,杀灭水中的病菌
一定温度、100g溶剂、饱和状态、以“克”为单位
外因 温度和压强
1.影响固体物质溶解度大小的因素有( )
A.①②⑤B.①②③ C.①④⑥ D.②⑥⑦
①溶质的性质 ②温度 ③压强 ④溶质的质量 ⑤溶剂的性质 ⑥溶解时是否搅拌或振荡 ⑦固体物质的颗粒大小
(1)“夏天晒盐”中的“盐”其溶解度可用图中________来表示(填“a ”“b ”或“c ”)。(2)在t1℃时,三种物质的溶解度大小关系是________。(3)在t2℃时,将40g的a放入50g水中充分搅拌,所得溶液质量为________g 。
2.(2019·青海中考)青海省柴达木盆地的察尔汗盐湖是我国最大的天然内陆咸水湖,当地农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。
3.【2020·新疆】X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )A.Y的溶解度为50 gB. T2 ℃时,X、Y两种物质的溶解度相等C. T1 ℃时,三种物质的溶解度由大到小的顺序是Y>X>ZD. T2 ℃时,50 g H2O与50 g X混合,可得到100 g X的饱和溶液
【点拨】没有指明温度,无法确定Y的溶解度,A错误;T2 ℃时,X、Y两种物质的溶解度均为50 g,溶解度相等,B正确;T1 ℃时,X、Y、 Z三种物质的溶解度由大到小的顺序是Y>X=Z,C错误;T2 ℃时,X的溶解度为50 g,T2 ℃时,50 g H2O与50 g X混合,最多只能溶解25 g X,则可得到75 g X的饱和溶液,D错误。
5.【2020·哈尔滨】如图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( ) A.t2 ℃时,甲的溶解度为70B.乙中含有少量的甲,可用蒸发溶剂的方法提纯乙C.t2 ℃时,甲、乙两种物质的溶液分别降温到t1 ℃,析出晶体的质量甲一定大于乙D.t2 ℃时,甲的溶液降温到t1 ℃,一定能得到甲的饱和溶液
【点拨】t2 ℃时,甲的溶解度为70 g,A不正确;乙的溶解度受温度变化影响较小,甲的溶解度受温度变化影响较大,乙中含有少量的甲,可用蒸发溶剂的方法提纯乙,B正确;由于不知道溶液质量及溶液是否饱和,故不能比较两种溶液析出固体的多少,C不正确;t2 ℃时,甲的溶液降温到t1 ℃,不一定能得到甲的饱和溶液,D不正确。
6.【2020·苏州】K2CO3、KNO3在不同温度时的溶解度及溶解度曲线如下。下列说法正确的是( )A. K2CO3的溶解度大于KNO3B.乙代表K2CO3的溶解度曲线C.t应在50~60 ℃之间D.40 ℃时,100 g KNO3饱和溶液中含63.9 g KNO3
【点拨】在不指明温度的情况下,无法比较溶解度的大小,A错误;根据溶解度曲线,结合表格数据可知,乙代表K2CO3的溶解度曲线,B正确;t应在60~80 ℃之间,C错误;40 ℃时,163.9 g KNO3饱和溶液中含63.9 g KNO3,D错误。
初中化学人教版九年级下册课题2 溶解度教学课件ppt: 这是一份初中化学人教版九年级下册课题2 溶解度教学课件ppt,共8页。PPT课件主要包含了探究问题,实验9-5,实验9-6,实验探究,剩余固体全部溶解,全部溶解,有固体剩余,有晶体析出,实验讨论,饱和溶液等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度课前预习ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度课前预习ppt课件,共8页。PPT课件主要包含了溶解度,溶解度四大理解要点,01g,P37活动与探究,几种物质的溶解度曲线等内容,欢迎下载使用。
初中化学人教版九年级下册第九单元 溶液课题2 溶解度图文ppt课件: 这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度图文ppt课件,共8页。PPT课件主要包含了NaCl,一定量,一定温度下,降温结晶,蒸发结晶等内容,欢迎下载使用。













