






高中化学第二节 氯及其化合物课文配套课件ppt
展开
这是一份高中化学第二节 氯及其化合物课文配套课件ppt,共30页。PPT课件主要包含了导入新课,NaCl,氯气的物理性质,刺激性气味,大量白烟,大量棕褐色烟,大量棕黄色烟,苍白色,归纳总结,有色布条不褪色等内容,欢迎下载使用。
1915年4月22日,德军在比利时的伊普尔战役中首次大规模使用毒气。当时战场出现了有利于德军的风向,德军打开了早已在前沿阵地屯集的装满氯气的钢瓶,一人多高的黄绿色烟云被每秒2~3米的微风吹向英法联军阵地。面对扑面而来的刺鼻的怪味,英法守军一阵大乱,阵线迅速崩溃。部分士兵用湿毛巾捂住嘴巴,他们逃往地势更高的地方,最终幸免于难。这次攻击,英法守军共中毒15000人,5000多人死亡,德军亦有数千人中毒和死亡。 这是战争史上的第一次化学战,从此,化学战作为最邪恶的战争被写入了战争的史册。
1.氯气为什么可以作为生化武器?2.为什么湿毛巾在一定程度上可以防止氯气中毒?湿毛巾上还可以蘸取什么溶液呢?3.为什么要逃往地势更高的地方呢?4.这其中包含了氯气的哪些性质呢?
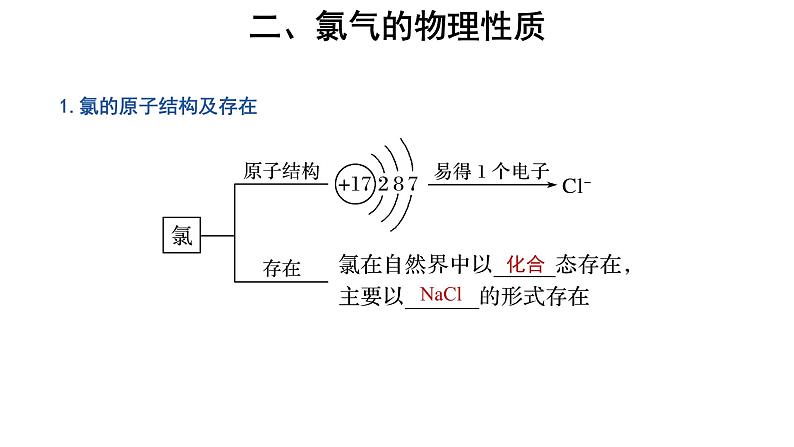
1.氯的原子结构及存在
例1 已知实验室制取氯气的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。结合氯气的物理性质,判断下列叙述是否正确。(1)加热盛有二氧化锰、浓盐酸的烧瓶,瓶内充满黄绿色气体( )(2)氯气的密度比空气大,常用向上排空气法收集氯气( )(3)闻氯气气味时,用手轻轻在集气瓶瓶口扇动,使极少量氯气飘进鼻孔( )(4)在充满氯气的集气瓶内加水,盖严后振荡,瓶内气体颜色变浅,液体变为黄绿色( )(5)氯气易液化,在低温和加压的条件下可以转变为液态(液氯)和固态( )
解析 氯气是黄绿色有强烈刺激性气味的有毒气体;氯气不仅可溶于水,而且还能与水反应,不能用排水法收集,常用向上排空气法收集。
例2 氯气可用于消灭田鼠,为此,可将氯气用软管通入到田鼠洞中,这是利用了氯气下列性质________(填序号)。①黄绿色 ②密度比空气大 ③有毒 ④易液化 ⑤可溶于水
解析 将氯气通入到田鼠洞中起灭鼠作用,一方面是利用其密度比空气大得多,可沉在洞底,另一方面是氯气有毒。
1.氯气与金属单质的反应写出下列反应的化学方程式,并指明主要反应现象:(1)与钠反应 ,产生 ;(2)与铁反应 ,产生 ;(3)与铜反应 ,产生 。
三、氯气与金属、非金属的反应
2.氯气与非金属单质氢气的反应:(1)在空气中点燃氢气,然后把导管伸入盛有氯气的集气瓶中。①观察到的现象是氢气在氯气中安静地 ,发出 火焰。②燃烧结束后,抽去盖在集气瓶口处的毛玻璃片,观察到的现象是集气瓶口上方出现 。③反应的化学方程式是 。(2)氯气和氢气的混合气体在强光照射时爆炸,产生此现象的原因是H2和Cl2混合后光照,反应瞬间完成,放出的热量使气体急剧膨胀而发生 。
(1)氯气是很活泼的非金属单质,具有很强的氧化性。①氯气能与绝大多数金属反应,把变价金属(如Fe、Cu)一般氧化到最高价。②氯气能与许多还原性化合物反应,如FeCl2溶液、KI溶液、SO2水溶液等。(2)燃烧是指发热发光的剧烈的化学反应。它强调的是①发光时也要发热;②反应剧烈;③实质是剧烈的氧化还原反应;④不一定要有氧的参加。
例3 下列化合物中,不能通过两种单质间化合直接制取的是A.FeCl3 B.CuCl2 C.HCl D.FeCl2
解析 Cl2与金属反应生成高价态的氯化物,所以FeCl2不能由两种单质直接化合制取。
例4 下列现象不属于H2在Cl2中燃烧现象的是A.苍白色火焰 B.瓶口有白雾C.集气瓶内气体颜色变浅 D.爆炸
解析 H2在Cl2中燃烧,发出苍白色火焰,瓶口因生成的HCl吸收空气中的H2O形成盐酸小液滴而形成白雾,瓶内气体颜色因Cl2的消耗而变浅,但不发生爆炸。
1.氯水的性质(1)氯气能溶于水,其水溶液俗称氯水。按照表中要求完成氯水的性质实验,将实验现象及有关结论填入表中:
(2)新制氯水具有漂白性是因为 ,反应的化学方程式是 ,该反应的氧化剂是 ,还原剂是 。
氯气与H2O反应生成了HClO
Cl2+H2O===HCl+HClO
2.次氯酸(HClO)的性质(1)次氯酸是 于水的弱酸,比碳酸酸性 ,写离子方程式时不能拆成离子形式。氯气和水反应的离子方程式: 。(2)次氯酸不稳定,见光易分解,反应的方程式: 。(3)次氯酸具有强氧化性,其氧化性比Cl2 ,可用于自来水的杀菌消毒,还可以用作漂白剂。
Cl2+H2O===H++Cl-+HClO
(1)光照氯水时,溶液中的次氯酸不断分解生成盐酸和氧气,溶液的浅黄绿色逐渐褪去,pH逐渐减小。(2)实验室中氯水需现用现配。保存氯水时,应避免光照、受热,实验室通常将氯水置于棕色试剂瓶中密封保存。
例5 下列关于氯水的叙述中正确的是A.新制氯水中只含Cl2和H2O分子B.新制氯水可使蓝色石蕊试纸先变红后褪色C.光照新制氯水有气泡逸出,该气体是Cl2D.新制氯水在密闭无色玻璃瓶中放置数天后酸性将减弱
解析 新制氯水成分的多样性决定了新制氯水性质上的多重性。新制氯水中主要含有三种分子H2O、Cl2、HClO和四种离子H+、Cl-、ClO-、OH-;新制氯水含有H+和HClO,蓝色石蕊试纸遇H+变红,变红后的试纸被HClO氧化褪色;光照新制氯水,发生反应2HClO 2HCl+O2↑,逸出的是O2而不是Cl2;该反应进行后,弱酸HClO转化为强酸HCl,在密闭无色玻璃瓶中不考虑HCl挥发,溶液的酸性增强。
例6 在新制氯水参加的反应中,有如下几种情况:(1)向氯化亚铁溶液中加入氯水,氯水中起作用的主要微粒是____,反应的离子方程式为_________________________。(2)向硝酸银溶液中加入氯水,氯水中起作用的主要微粒是_____,反应的离子方程式为____________________。(3)向氯水中滴加石蕊溶液,溶液变红,氯水中起作用的微粒是_____,然后又褪色,起作用的微粒是______。
解析 考查新制氯水成分的多样性,要从新制氯水所含的微粒种类(Cl2、HClO、H+、Cl-等)来考虑。
Cl2+2Fe2+===2Fe3++2Cl-
Ag++Cl-===AgCl↓
1.判断正误(正确的打“√”,错误的打“×”)(1)氯元素在自然界中既可以化合态存在,也可以游离态存在( )(2)氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物( )(3)氯气有毒,氯的化合物也都具有一定的毒性( )(4)氯气可以使湿润的有色布条褪色( )(5)氯气可以贮存在钢瓶中,说明Cl2与Fe不反应( )(6)Cl2具有很强的氧化性,在化学反应中只能作氧化剂( )(7)在NaClO溶液中通入CO2生成HClO,可证明碳酸酸性强于HClO( )(8)工业上制盐酸需要的HCl是通过H2和Cl2光照条件下生成的( )(9)任何物质的燃烧都必须有O2参与( )(10)物质有发热发光的变化一定是燃烧( )
解析 闻气体的方法是用手轻轻地在瓶口扇动,仅使少量的气体飘入鼻孔,不能直接用鼻子闻,A不正确;氯气密度比空气大,可用向上排空气法收集氯气,B不正确;氯气是一种有毒的气体,氯气会顺着风向扩散,疏散时应该逆着风向转移,C正确;氯气密度比空气大,泄漏时离地面越近氯气浓度越大,应尽量向高处逃生,D不正确。
2.下列说法中正确的是A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味B.用向下排空气法可以收集到纯净的氯气C.贮氯罐意外泄漏,应沿逆风方向疏散群众D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
3.下列关于氯气的叙述中正确的是A.钠在氯气中燃烧产生白烟B.红热的铜丝在氯气中燃烧生成CuClC.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰D.氯气的水溶液可以导电,说明氯气是电解质
解析 钠在氯气中燃烧,生成NaCl固体小颗粒,形成白烟,A项正确;红热的铜丝在氯气中燃烧生成CuCl2,B项错误;氢气在氯气中燃烧发出苍白色火焰,C项错误;Cl2是单质,既不是电解质,也不是非电解质,D项错误。
4.下列有关次氯酸的叙述不正确的是A.次氯酸不稳定,易分解B.次氯酸是一种强氧化剂C.次氯酸是弱酸,但酸性比碳酸强D.次氯酸能使染料和有机色质褪色
解析 HClO是一元弱酸,酸性比碳酸弱。
5.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是A.使红色布条褪色(HCl)B.将NaHCO3固体加入新制氯水,有无色气泡(H+)C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)D.滴加AgNO3溶液生成白色沉淀(Cl-)
解析 A项,次氯酸具有强氧化性,能氧化有色布条而使其褪色,与氯化氢无关,错误;B项,氯水显酸性,能与碳酸氢钠反应生成CO2气体,正确;C项,氯气氧化了亚铁离子生成三价铁离子,再滴加KSCN溶液,发现呈红色,正确;D项,氯离子和硝酸银反应生成氯化银白色沉淀,正确。
6.在第一次世界大战期间,有一次德军与英、法军在比利时对峙,黎明时,英、法军前线战壕的士兵突然看到一股黄绿色气体逐渐袭来,很快数百名英、法军战士窒息而死。后来人们在打扫战场时发现跑到山坡上的士兵竟幸免于难。(1)由上述事例可归纳出氯气的性质有_______________________________。(2)写出下列反应的化学方程式:①铁丝在氯气中燃烧:____________________。②铁粉溶于盐酸中:________________________。③少量的铁粉溶于氯水中:_______________________________________________。
黄绿色气体,有毒,密度比空气大
Fe+2HCl===FeCl2+H2↑
Fe+2HCl===FeCl2+H2↑,2FeCl2+Cl2===2FeCl3
(3)将新鲜的花瓣放入干燥的氯气中可观察到的现象是_________,原因是_________________________________________________________。(4)氯水久置或光照条件下均会变成稀盐酸,同时释放出氧气,说明次氯酸________,反应的化学方程式为_______________________。
瓣中含有水分,遇Cl2会产生HClO,HClO具有漂白性
相关课件
这是一份人教版 (2019)必修 第一册第二节 氯及其化合物评课ppt课件,共39页。
这是一份人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第二节 氯及其化合物备课课件ppt,共22页。PPT课件主要包含了氯水的成分,氯气与碱反应,你知道吗等内容,欢迎下载使用。
这是一份化学第二节 氯及其化合物说课ppt课件,共15页。PPT课件主要包含了新闻链接,氯气的物理性质,你知道吗等内容,欢迎下载使用。










