高中人教版 (新课标)第二节 元素周期律第1课时教案
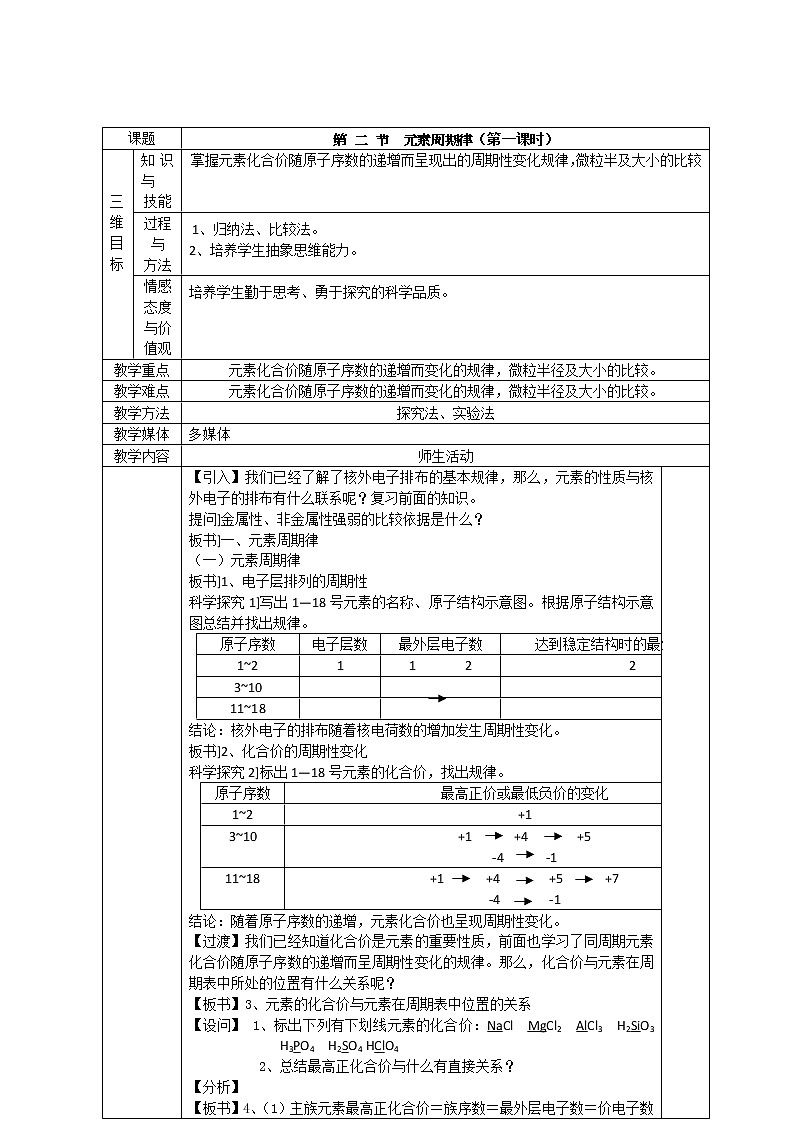
展开第 二 节 元素周期律(第一课时)
三
维
目
标
知识与
技能
掌握元素化合价随原子序数的递增而呈现出的周期性变化规律,微粒半及大小的比较
过程与
方法
1、归纳法、比较法。
2、培养学生抽象思维能力。
情感态度与价值观
培养学生勤于思考、勇于探究的科学品质。
教学重点
元素化合价随原子序数的递增而变化的规律,微粒半径及大小的比较。
教学难点
元素化合价随原子序数的递增而变化的规律,微粒半径及大小的比较。
教学方法
探究法、实验法
教学媒体
多媒体
教学内容
师生活动
【引入】我们已经了解了核外电子排布的基本规律,那么,元素的性质与核外电子的排布有什么联系呢?复习前面的知识。
提问]金属性、非金属性强弱的比较依据是什么?
板书]一、元素周期律
(一)元素周期律
板书]1、电子层排列的周期性
科学探究1]写出1—18号元素的名称、原子结构示意图。根据原子结构示意图总结并找出规律。
原子序数
电子层数
最外层电子数
达到稳定结构时的最外层电子数
1~2
1
1 2
2
3~10
11~18
结论:核外电子的排布随着核电荷数的增加发生周期性变化。
板书]2、化合价的周期性变化
科学探究2]标出1—18号元素的化合价,找出规律。
原子序数
最高正价或最低负价的变化
1~2
+1
3~10
+1 +4 +5
-4 -1
11~18
+1 +4 +5 +7
-4 -1
结论:随着原子序数的递增,元素化合价也呈现周期性变化。
【过渡】我们已经知道化合价是元素的重要性质,前面也学习了同周期元素化合价随原子序数的递增而呈周期性变化的规律。那么,化合价与元素在周期表中所处的位置有什么关系呢?
【板书】3、元素的化合价与元素在周期表中位置的关系
【设问】 1、标出下列有下划线元素的化合价:NaCl MgCl2 AlCl3 H2SiO3 H3PO4 H2SO4 HClO4
2、总结最高正化合价与什么有直接关系?
【分析】
【板书】4、(1)主族元素最高正化合价=族序数=最外层电子数=价电子数
【知识拓展】 1、价电子数:
上述规律只对主族元素成立,不适用于副族元素、零族元素。
【过渡】 写出下列化合物中有下划线元素的化合价:Na2CO3与CH4 H2SO4与H2S HCl与HClO4 分析最高正化合价与最低负化合价的关系,并解释其原因。
【分析】
【板书】5、(2)非金属元素,最高正化合价与最低负化合价绝对值之和等于8。
【反馈练习】 某元素X的最高价氧化物对应水化物的化学式为HXO4,则其气态氢化物的化学式为: ;
若其水溶液呈现酸性,且能与AgNO3溶液反应生成白色沉淀,则它在元素周期表中的位置是: 。
【分析】
板书] 6、原子半径的递变规律
元素符号
H
He
原子半径nm
0.037
元素符号
Li
Be
B
C
N
O
F
Ne
原子半径nm
0.152
0.089
0.082
0.077
0.075
0.074
0.071
元素符号
Na
Mg
Al
Si
P
S
Cl
Ar
原子半径nm
0.186
0.160
0.143
0.117
0.110
0.102
0.099
总结:同一周期,随着原子序数的递增,元素原子半径逐渐减小,呈现周期性变化。
练习]1、比较Na、S原子半径的大小。
2、比较Na、O原子半径的大小。
过渡]以上我们学习了原子半径大小的比较,那么离子半径的大小怎么比较呢?
(二)、微粒半径大小的比较
1、原子半径大小的比较
同主族,从上到下,原子半径逐渐增大。
同周期,从左到右,原子半径逐渐减小。
2、离子半径大小的比较
(1)具有相同电子层结构的离子半径大小的比较
电子层数相同,随着核电荷数的增加,原子核对核外电子的吸引能力增强,半径减小。
(2)同主族离子半径大小的比较
元素周期表中从上到下,电子层数逐渐增多,离子半径逐渐增大。
(3)同一元素的不同离子的半径大小比较
同种元素的各种微粒,核外电子数越多,半径越大,高价阳离子半径小于低价离子半径。
【反馈练习】
1.ⅦA族元素单质的沸点( );第三周期元素的最高正化合价( );IA族元素单质熔点( );F-,Na+,Mg2+,Al3+四种离子的离子半径( );同周期短周期元素的原子半径( ).
2.按粒子的半径从小到大顺序排列的是( )
A.Cl,S,P B.N,O,F C.Al3+,Mg2+,Na+ D.K,Na,Li
3.下列各组微粒中,按微粒半径依次增大排列的是( )
(A)Al3+,Al,Na,K (B)F,Cl,S2- ,S
(C)S2-,Cl - ,K + ,Ca 2+ (D)Mg,Si,P,K
4.a元素的阴离子,b元素的阴离子,c元素的阳离子具有相同的电子层结构,已知a的原子序数大于b的原子序数,则a,b,c三种离子半径大小的顺序是( )
A.a>b>c B.b>a>c C.c>a>b D.c>b>a
布置作业
《学案与测评》练习
板书设计
第 二 节 元素周期律
一、元素周期律
(一)元素周期律
1、电子层排列的周期性
2、化合价的周期性变化
3、元素的化合价与元素在周期表中位置的关系
4、(1)主族元素最高正化合价=族序数=最外层电子数=价电子数
5、(2)非金属元素,最高正化合价与最低负化合价绝对值之和等于8。
6、原子半径的递变规律
同一周期,随着原子序数的递增,元素原子半径逐渐减小,呈现周期性变化。
(二)、微粒半径大小的比较
1、原子半径大小的比较
同主族,从上到下,原子半径逐渐增大。
同周期,从左到右,原子半径逐渐减小。
2、离子半径大小的比较
(1)具有相同电子层结构的离子半径大小的比较
电子层数相同,随着核电荷数的增加,原子核对核外电子的吸引能力增强,半径减小。
(2)同主族离子半径大小的比较
元素周期表中从上到下,电子层数逐渐增多,离子半径逐渐增大。
3)同一元素的不同离子的半径大小比较
同种元素的各种微粒,核外电子数越多,半径越大,高价阳离子半径小于低价离子半径。
课后反思
本节课主要采用的是讨论法教学,在整个教学活动中始终注意学生学习的主动性,突出自主与合作的学习方式,充分调动了学生学习的积极性。
高中化学人教版 (新课标)必修2第二章 化学反应与能量第二节 化学能与电能第2课时教案设计: 这是一份高中化学人教版 (新课标)必修2第二章 化学反应与能量第二节 化学能与电能第2课时教案设计,共4页。教案主要包含了发展中的化学电源,原电池的定义 ,原电池电子的流向及正负极的判断,原电池电极反应的书写等内容,欢迎下载使用。
高中化学人教版 (新课标)必修2第一章 物质结构 元素周期律第三节 化学键第1课时教案: 这是一份高中化学人教版 (新课标)必修2第一章 物质结构 元素周期律第三节 化学键第1课时教案,共4页。教案主要包含了离子键,电子式等内容,欢迎下载使用。
高中化学人教版 (新课标)必修2第二节 元素周期律第2课时教案设计: 这是一份高中化学人教版 (新课标)必修2第二节 元素周期律第2课时教案设计,共4页。教案主要包含了反馈练习等内容,欢迎下载使用。













