





高考化学(人教)大一轮学考复习考点突破课件:第四章 非金属及其化合物 本章知识系统及重要化学方程式的再书写
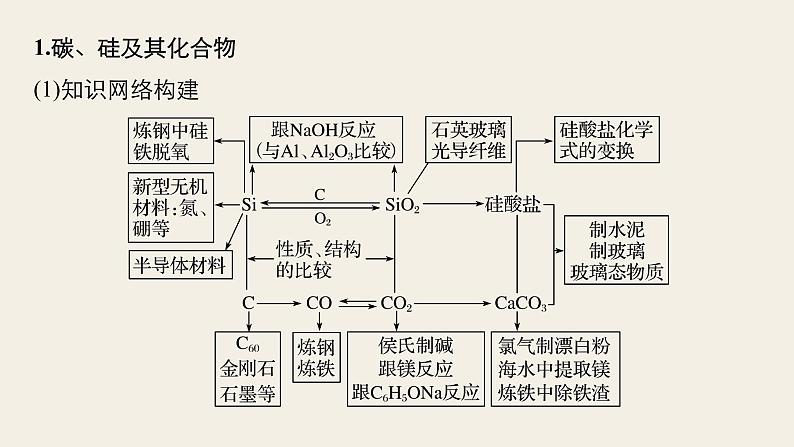
展开1.碳、硅及其化合物(1)知识网络构建
(2)重要反应必练写出下列反应的化学方程式,是离子反应的写离子方程式。①Si和NaOH溶液的反应 ;②SiO2和NaOH溶液的反应 ;③SiO2和C的反应 ;
④SiO2和氢氟酸的反应 ;⑤向Na2SiO3溶液中通入过量CO2气体 ;⑥Mg在CO2中燃烧 ;⑦向澄清石灰水中通入少量CO2气体 ;
Ca2++2OH-+CO2===CaCO3↓+H2O
SiO2+4HF===SiF4↑+2H2O
⑧向澄清石灰水中通入过量CO2气体 ;⑨除去CO2中的CO ;⑩生产普通玻璃的原理 、 。
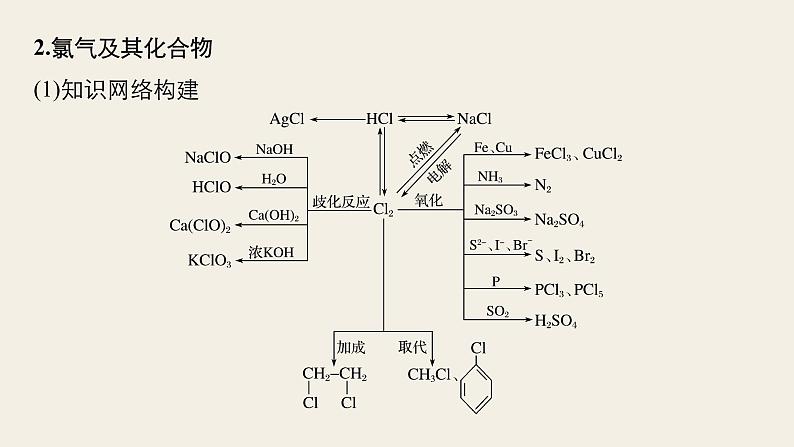
2.氯气及其化合物(1)知识网络构建
(2)重要反应必练写出下列反应的化学方程式,是离子反应的写离子方程式。①Cl2和H2O的反应 ;②Cl2和NaOH溶液的反应 ;③Cl2和石灰乳的反应 ;④把Cl2通入到Na2SO3溶液中 ;
Cl2+H2OH++Cl-+HClO
Cl2+Ca(OH)2===Ca2++Cl-+ClO-+H2O
Cl2+2OH-===Cl-+ClO-+H2O
⑤将Cl2和SO2混合通入H2O中 ;⑥将Cl2通入到氢硫酸溶液中 ;⑦将浓盐酸和MnO2混合加热 ;⑧电解饱和食盐水 ;
Cl2+H2S===S↓+2H++2Cl-
SO2+Cl2+2H2O===4H++2Cl-+
⑨将浓盐酸与漂白液混合 ;⑩将浓盐酸与KClO3溶液混合 ;⑪向KMnO4固体滴加浓盐酸 ;⑫向漂白粉溶液中通入少量CO2气体 。
6H++5Cl-+ ===3Cl2↑+3H2O
Cl-+ClO-+2H+===Cl2↑+H2O
+16H++10Cl-===2Mn2++5Cl2↑+8H2O
Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO
3.硫及其化合物(1)知识网络构建
(2)重要反应必练写出下列反应的方程式,是离子反应的写离子方程式。①S溶于热的烧碱溶液生成两种钠盐 ;②把H2S气体通入CuSO4溶液中 ;③Na2S溶液在空气中放置变浑浊 ;
2S2-+O2+2H2O===2S↓+4OH-
H2S+Cu2+===CuS↓+2H+
④铜丝在硫蒸气中燃烧 ;⑤将SO2气体通入到氢硫酸中 ;⑥把H2S气体通入到FeCl3溶液中 ;⑦SO2通入足量的澄清石灰水中 ;⑧SO2通入溴水中,使溴水褪色 ;
SO2+2H2S===3S↓+2H2O
H2S+2Fe3+===S↓+2Fe2++2H+
SO2+Br2+2H2O=== +2Br-+4H+
SO2+Ca2++2OH-===CaSO3↓+H2O
⑨用足量氨水吸收SO2尾气 ;⑩Cu和浓硫酸的反应 ;⑪C和浓硫酸的反应 ;⑫把浓H2SO4滴到Na2SO3固体上 。
H2SO4(浓)+Na2SO3===Na2SO4+H2O+SO2↑
4.氮及其化合物(1)知识网络构建
(2)重要反应必练写出下列反应的方程式,是离子反应的写离子方程式。①N2和H2的反应 ;②把NH3通入水中 ;③实验室利用NH4Cl固体、Ca(OH)2固体混合加热制备NH3 ;
④NH3的催化氧化 ;⑤NH4HCO3溶液中加入过量稀NaOH溶液 ;⑥NO2溶于水 ;⑦NO2被烧碱溶液吸收生成两种钠盐 ;
⑧物质的量之比为1∶1的NO和NO2混合气体恰好被烧碱溶液吸收生成一种钠盐 ;⑨Cu和稀HNO3的反应 ;⑩Cu和浓HNO3的反应 ;
高考化学(人教)大一轮学考复习考点突破课件:第四章 非金属及其化合物 第16讲: 这是一份高考化学(人教)大一轮学考复习考点突破课件:第四章 非金属及其化合物 第16讲,共60页。PPT课件主要包含了课时作业,硫化物,硫酸盐,还原氧化,酸性氧化物的通性,含硫化石燃料,金属矿物,BaSO4,BaSO3,品红溶液等内容,欢迎下载使用。
高考化学(人教)大一轮学考复习考点突破课件:第四章 非金属及其化合物 第15讲: 这是一份高考化学(人教)大一轮学考复习考点突破课件:第四章 非金属及其化合物 第15讲,共60页。PPT课件主要包含了课时作业,氯气的物理性质,刺激性,2与非金属反应,CaClO2,Cl2,HClO,Cl-,ClO-,OH-等内容,欢迎下载使用。
高考化学(人教)大一轮学考复习考点突破课件:第三章 金属及其化合物 本章知识系统及重要化学方程式再书写: 这是一份高考化学(人教)大一轮学考复习考点突破课件:第三章 金属及其化合物 本章知识系统及重要化学方程式再书写,共13页。












