


高中人教版 (新课标)第三节 盐类的水解教课内容课件ppt
展开
这是一份高中人教版 (新课标)第三节 盐类的水解教课内容课件ppt,共33页。PPT课件主要包含了思考与交流,C时成立,盐溶液不一定显中性,探究主题,盐溶液的酸碱性,讨论·分析,盐类水解的定义,温故而知新,课堂练习,结论“越弱越水解”等内容,欢迎下载使用。
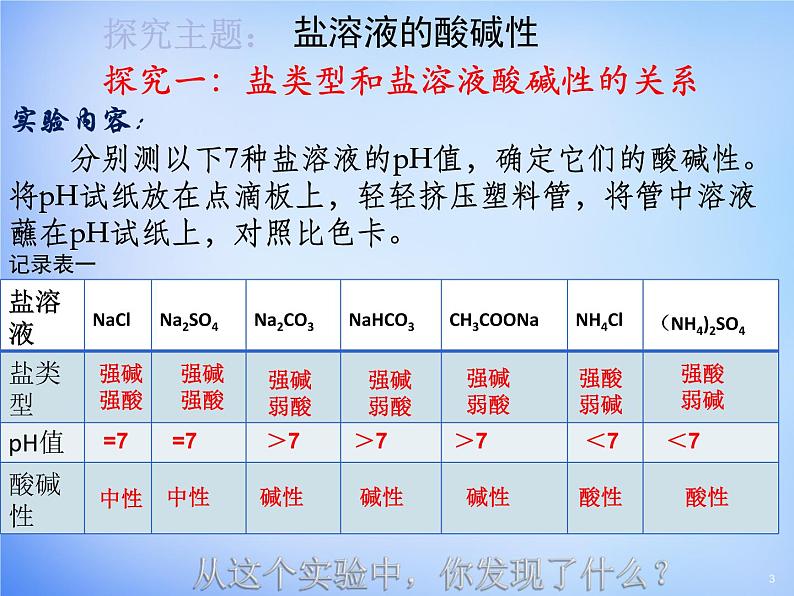
1、pH>7的溶液呈碱性,pH=7的溶液呈中性,pHNaAc>Na2SO4>(NH4)2SO4>NaHSO4
2、比较盐溶液中各离子浓度的相对大小时,当盐中含有易水解的离子,需考虑盐的水解。练:25℃时,在浓度均为1m/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2三种溶液中,若测得其中[NH4+]分别为a、b、c(单位为ml/L),则下列判断正确的是( ) A.a=b=c B.c>a>b C.b>a>c D.a>c>b
3、判断溶液中离子能否大量共存(了解) 弱酸根离子与弱碱阳离子在水溶液中互相促进水解,水解程度增大。有些双促水解反应不能完全进行,这些离子能够共存;有些双促水解反应能完全进行则称为“双水解反应”。如:完全双水解特例:① Al3+与HCO3- 、CO32- 、ClO- 、S2- 、HS- 、AlO2-等发生完全双水解,生成沉淀或气体。② Fe3+与HCO3- 、CO32- 、AlO2-等。③ NH4+与SiO32-等发生完全双水解 不能在溶液中大量共存。
玻璃筒里面放入的什么药品?
外筒(钢质)放入的是什么药品?
泡沫灭火器里的药品是NaHCO3溶液和Al2(SO4)3溶液。
泡沫灭火器工作原理(了解): 泡沫灭火器中的反应物分别是硫酸铝溶液和碳酸氢钠溶液,它们是如何产生二氧化碳的?Al3+ + 3H2O Al(OH)3 + 3H+HCO3- + H2O H2CO3 + OH-混合时, H+ + OH- H2O两个水解平衡相互促进, Al(OH)3形成沉淀, H2CO3 分解为CO2,总反应为:Al3+ + 3HCO3- = Al(OH)3 ↓+3CO2↑
4、某些易水解盐溶液的配制例:配制FeCl3溶液,由于: Fe3+ + 3H2O Fe(OH)3 +3H+ 因生成难溶的Fe(OH)3而得不到澄清溶液,可加入少量盐酸以防止浑浊,如何防浑浊?(加少量硫酸可以吗?)。 配制FeCl3、SnCl2等溶液时,先用少量浓盐酸溶解 ,再加水稀释到所需的浓度。为什么?
5、选择制备盐的途径时,需考虑盐的水解。如制备Al2S3时,因无法在溶液中制取,会完全水解,只能由干法直接反应制取。 加热蒸干AlCl3、MgCl2、FeCl3等溶液时,得不到AlCl3、MgCl2、FeCl3晶体,必须在蒸发过程中不断通入HCl气体,以抑制FeCl3的水解,才能得到其固体。请解释?
6、化肥的合理使用,有时需考虑盐的水解。如:铵态氮肥和草木灰不能混合施用,因草木灰(有效成分K2CO3)水解呈碱性。7、某些试剂的实验室存放,需要考虑盐的水解。如:Na2CO3、Na2SiO3等水解呈碱性,不能存放在磨口玻璃塞的试剂瓶中;NH4F不能存放在玻璃瓶中,因为NH4F水解应会产生HF,腐蚀玻璃 。
8、溶液中,某些离子的除杂,需考虑盐的水解。练习:为了除去氯化镁酸性溶液中的Fe3+离子,可在加热搅拌下加入一种试剂,过滤后再加入适量盐酸。这种试剂是( ) A.氧化镁 B.氢氧化钠 C.碳酸钠 D. 碳酸镁
9、明矾净水 KAl(SO4)·12H2O氯化铁也能净水,原理与明矾一样。练习:1、某些活泼金属(如镁)与强酸弱碱盐(如NH4Cl)溶液反应为什么能产生H2?2、书后溶解性表中,为何在提到Al2(CO3)3和Fe2(CO3)3时显示的是“ — ”?
五、盐溶液中离子浓度间关系
“三个守恒”:以Na2CO3溶液为例。⒈电荷守恒:因溶液是电中性的,所以溶液中阳离子所带的正电荷总数与阴离子所带负电荷总数相等。c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)⒉物料守恒:关键元素的原子数目守恒。c(Na+)=2[c(CO32-)+ c(HCO3-)+c(H2CO3)](碳元素守恒)⒊质子守恒(水的电离守恒):c(OH-)=c(H+)+ c(HCO3-)+2c(H2CO3)
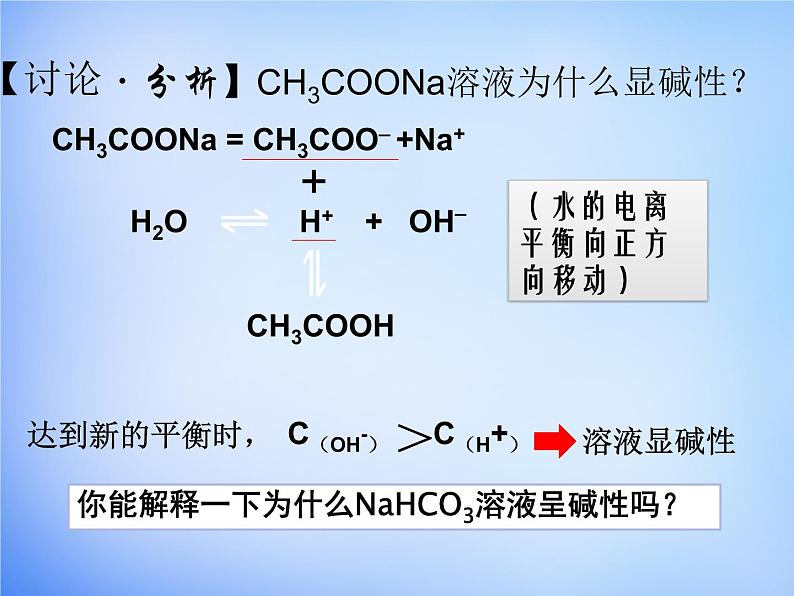
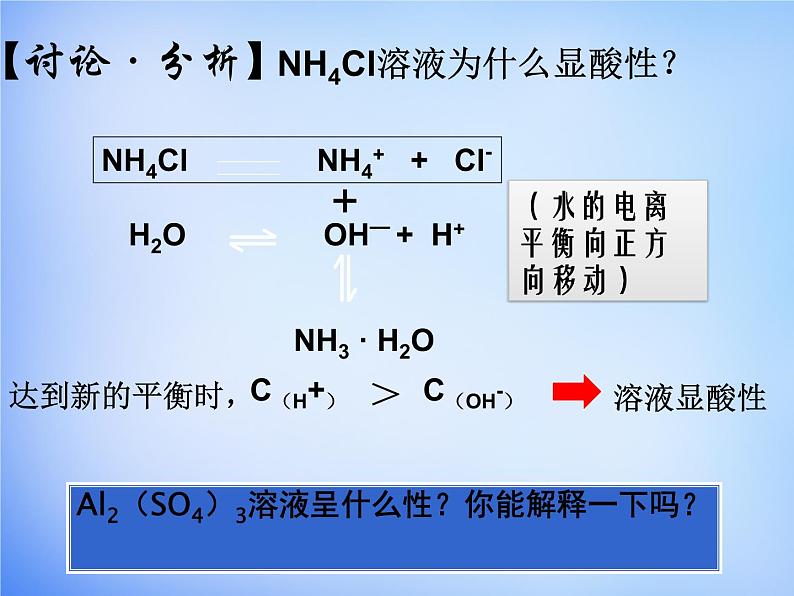
“大小比较”⒈ CH3COONa溶液有那些离子,大小如何?c(Na+)>c(CH3COO-)>c(OH-)>c(H+)⒉Na2CO3溶液有那些离子?大小如何?c(Na+)>c(CO32-)> c(OH-)>c(HCO3-)> c(H+)⒊NH4Cl溶液有那些离子?大小如何?c(Cl-)>c(NH4+)> c(H+)>c(OH-)练习:已知等物质的量浓度醋酸与醋酸钠混合溶液呈酸性,写出混合溶液中各离子浓度大小关系。
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
相关课件
这是一份人教版 (新课标)选修4 化学反应原理第三节 盐类的水解备课课件ppt,共23页。PPT课件主要包含了盐类水解平衡影响因素,HCl,课堂练习一,盐类水解的应用,合作探究,课堂练习三,课堂练习四,课堂练习五,电离方程式,水解方程式等内容,欢迎下载使用。
这是一份高中化学人教版 (新课标)选修4 化学反应原理第三节 盐类的水解授课ppt课件,共52页。PPT课件主要包含了①③④,课堂练习,解题指导,例题分析等内容,欢迎下载使用。
这是一份人教版 (新课标)选修4 化学反应原理第三节 盐类的水解课堂教学课件ppt,共51页。PPT课件主要包含了知识回顾,实验记录,学习反思,盐类的水解,课堂练习一,课堂小结,学习目标,学习难点,①③④,学习新知等内容,欢迎下载使用。










