




中考化学专项复习课件 专项06 氢氧化钠变质的探究 课件
展开1.下列物质的溶液长期敞口放置在空气中(不考虑水分的蒸发),溶液质量因发生化学变化而增大的是( )
类型一 氢氧化钠是否变质的探究
A.浓盐酸B.氯化钾溶液C.浓氨水D.氢氧化钠溶液
[解析] 浓盐酸、浓氨水在空气中分别挥发出氯化氢气体、氨会使溶液质量减小;氯化钾在空气中无变化,溶液质量不变;氢氧化钠会吸收空气中的二氧化碳生成碳酸钠,发生化学变化导致溶液质量增加。
2.已知NaOH容易与空气中的CO2作用而变质。小军同学在实验室发现一瓶敞口放置的NaOH固体后,设计方案,对这瓶NaOH固体变质情况进行了如下实验探究: (1)上述实验操作的名称分别是:① ,④ 。 (2)根据上述实验,可以确定该固体 (填“已”或“未”)变质。 (3)步骤③中加过量氯化钙溶液的目的是 。 (4)若测得E的pH=7,则A的成分是 ,若测得E的pH>7,则A的成分是 。
3.某学习小组测定实验室里一瓶NaOH溶液是否变质,以及变质程度,进行了下列实验,实验方案正确的( )A.取少量样品,加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液没有变质B.取少量样品,加入少量稀盐酸,没有气泡产生,证明氢氧化钠溶液没有变质C.取少量样品,加入过量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液不变色,证明氢氧化钠溶液完全变质D.取少量样品,加入过量的氢氧化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液部分变质
类型二 氢氧化钠变质程度的探究
[解析] 碳酸钠和氢氧化钠都显碱性,都能使酚酞溶液变色;氢氧化钠部分变质成碳酸钠,若滴加少量的稀盐酸,氢氧化钠和盐酸先反应生成氯化钠和水,也不会出现气泡;加入氢氧化钡会引入氢氧根离子,对氢氧化钠的检验造成干扰。
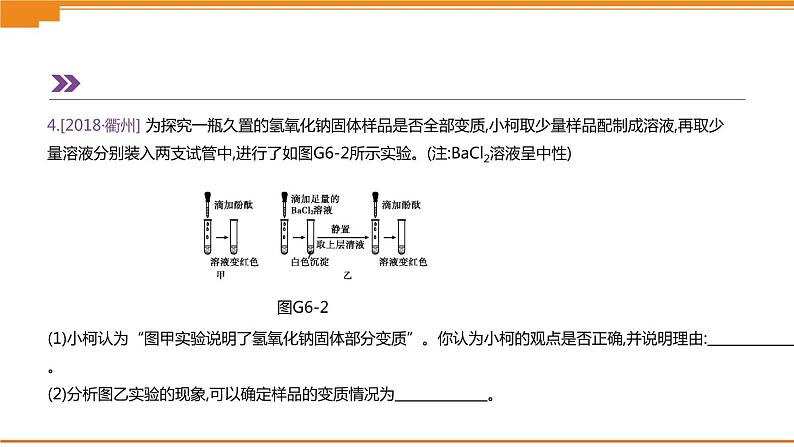
4.[2018·衢州] 为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如图G6-2所示实验。(注:BaCl2溶液呈中性)
(1)小柯认为“图甲实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由: 。 (2)分析图乙实验的现象,可以确定样品的变质情况为 。
(3)进一步探究:另取少量样品溶液,加入一定质量分数的稀盐酸,直至过量。请在图G6-3中画出“生成CO2的质量随加入稀盐酸质量变化”的大致图像。
[答案] (1)不正确,氢氧化钠和碳酸钠溶液均显碱性,无论氢氧化钠是否变质,都能使无色酚酞溶液变红色(2)部分变质 (3)
[解析] (1)小柯的观点不正确;氢氧化钠固体露置在空气中,会发生潮解,能吸收空气中的二氧化碳气体生成碳酸钠和水而变质,碳酸钠属于盐,其水溶液显碱性,碳酸钠溶液能使无色酚酞溶液变红色;氢氧化钠属于碱,其溶液能使无色酚酞溶液变红色。所以,甲实验中,不论氢氧化钠是否变质,溶液都会变为红色。(2)乙实验中,向样品溶液中加入氯化钡溶液产生白色沉淀,证明溶液中含有碳酸钠,因为碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠;由于加入足量的氯化钡溶液,碳酸钠被完全反应,生成的氯化钠及过量的氯化钡的溶液均显中性,静置后取上层清液,滴加酚酞溶液,酚酞溶液变红色,证明溶液中含有氢氧化钠,样品中含有氢氧化钠和碳酸钠,故氢氧化钠部分变质。(3)向样品中加入稀盐酸,盐酸先与氢氧化钠反应生成氯化钠和水,该反应无气体产生;当氢氧化钠完全反应后,盐酸继续和碳酸钠反应生成氯化钠、二氧化碳和水;当碳酸钠完全反应后,再加稀盐酸,无气体产生。生成二氧化碳质量随加入盐酸质量变化的图像如下:
5.[2018·巴中] 小明在实验室发现一瓶未密封的KOH固体,对其成分进行实验探究。查阅资料 ①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因 。 ②K2CO3溶液呈碱性,CaCl2溶液、KCl溶液呈中性。猜想假设 假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3。进行实验
拓展应用 完全变质的KOH也有利用价值,从K2CO3的组成或性质看,K2CO3在农业上的用途是 (填一种即可)。
中考化学二轮复习专题课件- 氢氧化钠变质的探究 (含答案): 这是一份中考化学二轮复习专题课件- 氢氧化钠变质的探究 (含答案),共16页。PPT课件主要包含了氢氧化钠是否变质了,课堂练习一,氢氧化钠没有变质,氢氧化钠全部变质,氢氧化钠部分变质,种情况,只有NaOH,只有Na2CO3,课堂练习二,课堂练习三等内容,欢迎下载使用。
中考化学二轮专题复习专题课件:氢氧化钠变质的探究 (含答案): 这是一份中考化学二轮专题复习专题课件:氢氧化钠变质的探究 (含答案),共16页。PPT课件主要包含了氢氧化钠是否变质了,课堂练习一,氢氧化钠没有变质,氢氧化钠全部变质,氢氧化钠部分变质,种情况,只有NaOH,只有Na2CO3,课堂练习二,课堂练习三等内容,欢迎下载使用。
2023年中考化学二轮专题复习氢氧化钠变质的探究课件: 这是一份2023年中考化学二轮专题复习氢氧化钠变质的探究课件,共15页。PPT课件主要包含了合作探究,小组讨论,交流反思,课堂小结等内容,欢迎下载使用。












