




中考化学专项复习课件 专项08 盐的化学性质 课件
展开1.[2018·黔东南] 下列各种溶质的溶液混合后无明显现象的一组是( )A.HCl、Na2CO3、 K2SO4B.KNO3、Ba(OH)2、 NaClC.KCl、AgNO3、HNO3D.NaOH、FeCl3、(NH4)2SO4
类型一 盐类物质的相互反应
[解析] HCl与Na2CO3能反应生成气体;KCl与AgNO3反应生成白色沉淀;NaOH与FeCl3反应生成红褐色沉淀,NaOH与(NH4)2SO4反应会生成气体。
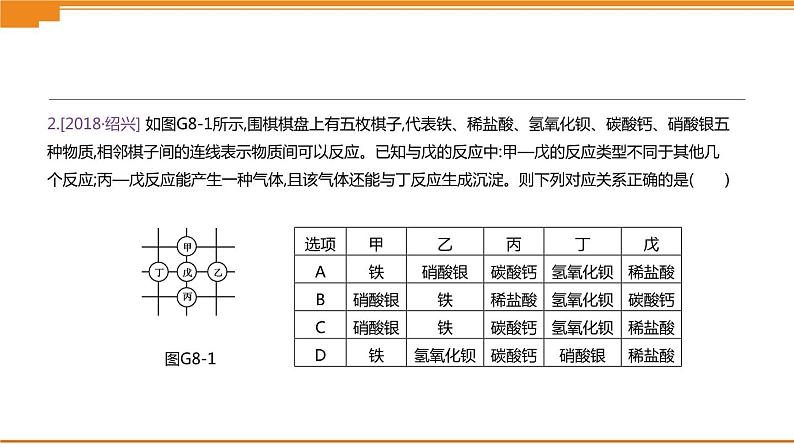
2.[2018·绍兴] 如图G8-1所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钡、碳酸钙、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中:甲—戊的反应类型不同于其他几个反应;丙—戊反应能产生一种气体,且该气体还能与丁反应生成沉淀。则下列对应关系正确的是( )
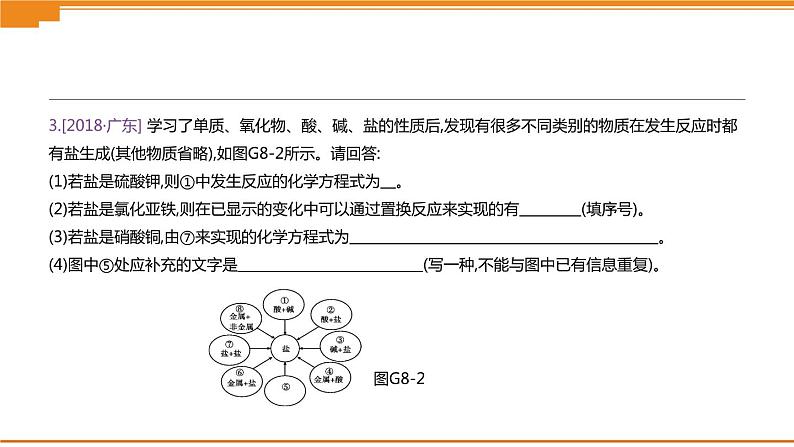
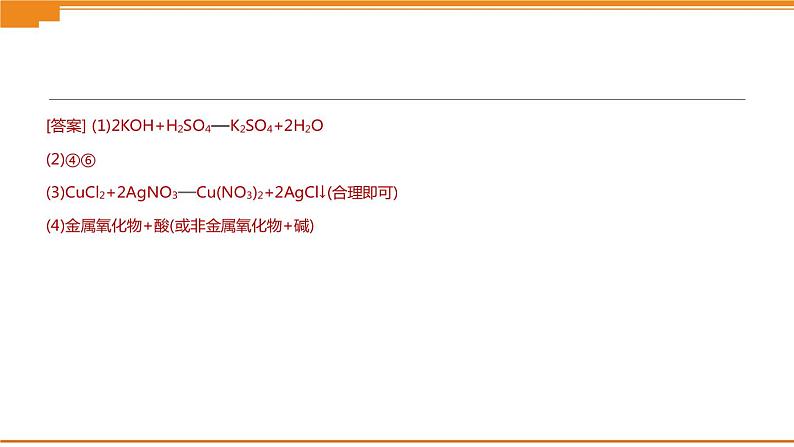
3.[2018·广东] 学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图G8-2所示。请回答: (1)若盐是硫酸钾,则①中发生反应的化学方程式为 。 (2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有 (填序号)。 (3)若盐是硝酸铜,由⑦来实现的化学方程式为 。 (4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
4.[2018·长春] 图G8-3表示物质间的转化关系(图中“→”表示某种物质转化成另一种物质)。(1)转化①的基本反应类型是 反应。 (2)向澄清石灰水中通入CO2能够实现转化②,反应的化学方程式为 。 (3)若转化③、④、⑤都是与同种物质反应生成CaCl2,则该物质是 。
类型二 物质或离子间的共存
5.[2018·宿迁] 下列各组离子在水溶液中,能大量共存的是( )A.Cu2+、Mg2+、N、OH-B.H+、S、C、Ba2+C.K+、N、Cl-、Na+D.H+、N、Ca2+、 OH-
[解析] 本题主要考查离子共存问题。A中Cu2+、Mg2+和OH- 结合分别生成氢氧化铜和氢氧化镁沉淀,不能大量共存,故A不符合题意;B中H+和C结合成水和二氧化碳,S、C和Ba2+结合成硫酸钡沉淀和碳酸钡沉淀,不能大量共存,故B不符合题意;C中K+、N、Cl-、Na+彼此不形成沉淀、气体或水,能大量共存,故C符合题意;D中H+和 OH-结合成水,不能大量共存,故D不符合题意。
6.[2017·泰安] 下列物质能在pH=13的无色溶液中大量共存的是( )A.NaNO3、NaCl、KNO3、(NH4)2SO4B.H2SO4、HCl、AgNO3、Na2SO4C.KMnO4、CuCl2、Fe2(SO4)3、NaNO3D.K2SO4、NaCl、K2CO3、NaOH
7.[2018·济宁] 某工业园区甲、乙两化工厂排放的废水中含有K+、Cu2+、Fe3+、Cl-、OH-、N六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质带来严重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水呈碱性。(1)甲厂废水中一定含有的离子是 ,可能含有的离子是 。 (2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是 (填离子符号),过滤后的废水中主要含有 (填化学式)两种物质,处理后的废水符合排放标准。
(1)OH-、K+ Cl-或N(2)Cu2+、Fe3+、OH- KCl、KNO3
[解析] 本题考查离子之间的共存问题,如果离子间发生化学反应,则不能大量共存,反之是可以的。(1)甲厂废水呈碱性,一定含有OH-,Cu2+、Fe3+与OH-结合生成沉淀,故不存在,则一定存在K+,另一种离子可以是Cl-或N。(2)在这六种离子中,OH-与Cu2+ 、Fe3+结合生成沉淀,剩下的离子构成KCl、KNO3。
8.[2018·烟台] 下列各组物质的溶液,不用其他试剂,只用观察和组内物质相互混合的方法,不能将它们一一鉴别的是( )A.HCl NaOH FeCl3 NaClB.H2SO4 NaCl Na2CO3 CaCl2C.NaNO3 HCl CaCl2 KOHD.MgCl2 KOH Cu(NO3)2 Na2SO4
[解析] C中四种溶液均为无色,采用互滴法,均无明显现象,四组现象完全相同,无法鉴别。
9.[2018·呼和浩特] 根据大量的实验总结得出,酸碱盐之间相互发生复分解反应的条件是:生成物中有沉淀、气体或水。依据该条件,某化学小组的同学推断,稀硫酸和氯化镁溶液不能发生复分解反应。为了进一步确认该推断的可靠性,该小组同学将一定量的稀硫酸和一定量氯化镁溶液在烧杯中混合后,进行了如下探究活动。(1)甲同学取烧杯中混合溶液,分别进行以下两个实验,记录实验现象如下,请依据实验现象填写实验结论。
(2)乙同学看到甲同学的实验报告后,认为甲同学的结论不正确,原因是 。为了进一步确认两者没有发生反应,还需检验烧杯内的混合液中是否含有氯化镁,于是乙同学设计了如下两个实验。 ①取少量烧杯内的混合液于试管中,逐滴加入过量的 溶液,证明了混合溶液中含有Mg2+,整个实验过程中乙同学观察到的实验现象是 ; ②乙同学另取少量烧杯内的混合液,通过实验成功的检验出混合溶液中含有Cl-。他设计的方案为 (写出操作和现象)。 总结 通过上述实验,该小组同学证明了稀硫酸和氯化镁溶液确实没有发生反应。
[解析] (1)向溶液中滴加石蕊溶液,溶液变红,说明溶液呈酸性,说明溶液中含有氢离子,离子符号为H+;向溶液中加入氯化钡溶液,有白色沉淀产生,说明溶液中含有硫酸根离子,离子符号为S。(2)甲同学的结论不正确,如果硫酸过量,则溶液中的氯化镁已经和硫酸完全反应完,过量的硫酸会与氯化钡发生反应。①取少量烧杯内的混合液于试管中,逐滴加入过量的氢氧化钠或氢氧化钾溶液,溶液中先无明显现象,一段时间后有白色沉淀产生,证明了混合液中含有镁离子;②另取少量烧杯内的混合液于试管中,先加过量的硝酸钡溶液,过滤,再向滤液中滴加硝酸银溶液,溶液中有白色沉淀产生,则混合液中含有氯离子。
[答案](1)H+ S(2)还可能是反应后硫酸有剩余①氢氧化钠(或氢氧化钾) 先无明显现象,一段时间后有白色沉淀产生②另取少量烧杯内的混合液于试管中,先加过量的硝酸钡溶液,过滤,再向滤液中滴加硝酸银溶液,溶液中有白色沉淀产生
类型四 混合物中盐的含量测定
10.[2018·威海] 某纯碱厂生产的某批次碳酸钠产品中可能含有氯化钠杂质。定性检验(1)要确定该产品中是否含有杂质氯化钠,你的方法是 。 定量测定(2)若利用沉淀法测定该产品中碳酸钠的质量分数,你确定的反应原理是 (用化学方程式表示)。 (3)假设你取样的质量为m1,根据你确定的反应原理,你需要通过实验测量沉淀 (填化学式)的质量(假设你测得的沉淀的质量为m2)。
(4)请你设计实验方案,获得数据m1、m2,把方案填在下表中。
(5)数据处理请用含m1、m2的式子表示所测样品中碳酸钠的质量分数: 。 分析讨论(6)要测定混合物中某成分的含量,可通过化学方法将不易测定的物质转化为易测量的物质。除沉淀法外,还可依据反应: (用化学方程式表示)来测定该纯碱样品中碳酸钠的质量分数。
中考化学专项复习课件 专项12 化学方程式集锦 课件: 这是一份中考化学专项复习课件 专项12 化学方程式集锦 课件,共14页。
中考化学专项复习课件 专项10 物质的分类 课件: 这是一份中考化学专项复习课件 专项10 物质的分类 课件,共11页。PPT课件主要包含了答案D,图G10-1,答案C,图G10-2,答案A,图G10-3,答案B等内容,欢迎下载使用。
中考化学专项复习课件 专项09 化学用语 课件: 这是一份中考化学专项复习课件 专项09 化学用语 课件,共20页。PPT课件主要包含了类型一元素符号,答案C,答案A,图G9-1,答案B,图G9-2,图G9-3,类型三离子符号,图G9-4,图G9-5等内容,欢迎下载使用。












