


高考化学一轮复习方案_第5讲-氧化还原反应
展开1.了解氧化还原反应的本质是电子的转移。 2.了解常见的氧化还原反应,能判断反应中的氧化剂、还原剂、氧化产物、还原产物。 3.能判断氧化还原反应中电子转移的方向和数目。 4.掌握物质氧化性、还原性强弱的比较方法。 5.能运用原子守恒、得失电子守恒、电荷守恒,进行氧化还原反应的有关计算。
► 探究考向一 氧化还原反应基本概念 —— 知 识 梳 理 —— 1.氧化还原反应的本质及特征 (1)本质:反应过程中___________________________________。 (2)特征:反应前后元素的化合价_______________。
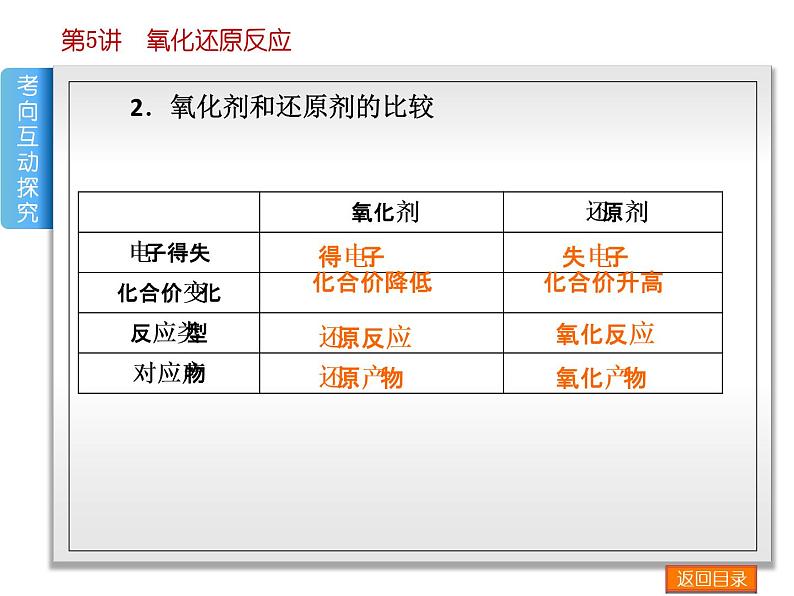
2.氧化剂和还原剂的比较
4.电子转移的表示Cu与稀硝酸反应中电子转移的方向和数目可表示为:(1)单线桥法:______________________________________________。(2)双线桥法:______________________________________________。
自主提问 有单质参加或生成的反应一定是氧化还原反应吗?
5.氧化产物、还原产物氧化产物是指__________________________________的生成物。还原产物是指________________________________的生成物。6.氧化性、还原性氧化性是指物质________电子的性质。还原性是指物质________电子的性质。
还原剂失去电子被氧化后
氧化剂得到电子被还原后
自主提问 如何判断氧化剂、还原剂、氧化产物、还原产物?
【触摸高考】 高考选项正误判断
—— 核心突破 ——
—— 典例精析 ——
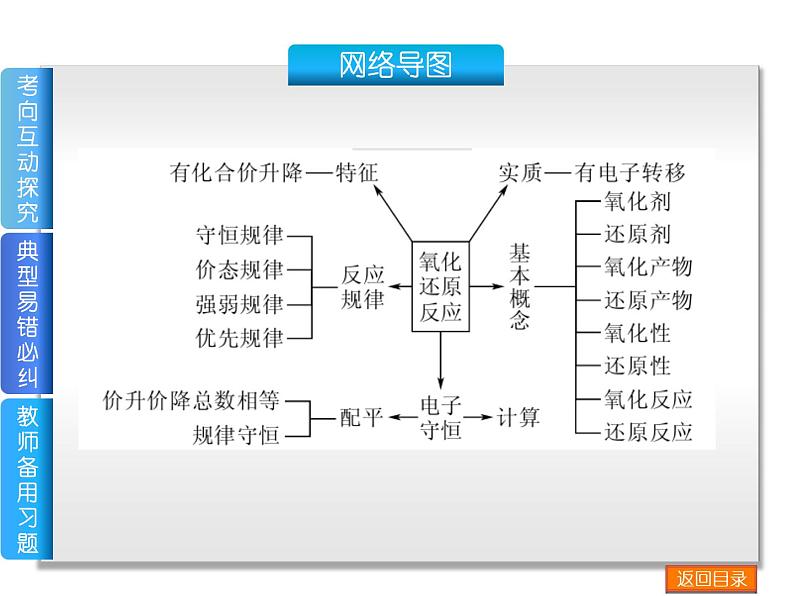
► 探究考向二 氧化还原反应的有关计算 —— 知 识 梳 理 —— 一、书写氧化还原方程式遵循的一般规律1.守恒规律氧化剂获得的电子总数=_______________________。2.价态规律同种元素不同价态之间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→________”,而不会出现交叉现象。图示如下:
如反应KClO3+6HCl===KCl+3Cl2↑+3H2O中,转移的电子数为5,而非6。可总结为:只靠近,不交叉,相邻价态不反应。
3.优先规律在浓度相差不大的溶液中:(1)同时含有几种还原剂时____________优先被氧化。(2)同时含有几种氧化剂时____________优先被还原。4.强弱规律氧化还原反应的发生,总是较强氧化性的氧化剂跟较强还原性的还原剂反应,生成________的还原产物和________的氧化产物。
二、氧化还原反应方程式的配平——化合价升降法
► 易错 4 概念混淆 判断失误
[易错提示] ①氧化剂、氧化产物、被氧化概念之间的对应关系易混淆;②不清楚硫酸的作用。 [试答] ________
提升 此类题看似简单,实际由于考生概念混淆很容易判断错误,例如KClO3是氧化剂,其对应的产物往往错判成氧化产物,等等。所以准确理解概念,用对比、联系的方法加以深化很重要。这里提示同学们,氧化还原反应的概念都是成对的,只需掌握一半即可,如“失电——(被)氧化——还原剂——氧化产物它变去——价升特征记心里”就可以很好的帮助同学们清楚掌握这些概念而不易混淆。另外,有许多氧化剂需要用硫酸酸化,因为浓硫酸有强氧化性,学生往往误认为硫酸的作用是氧化剂,实际就是起酸性作用。
【备选理由】 考查氧化还原反应的相关概念和离子方程式。
新高考化学一轮复习课件 第1章 第5讲 氧化还原反应的计算与方程式的配平: 这是一份新高考化学一轮复习课件 第1章 第5讲 氧化还原反应的计算与方程式的配平,共55页。PPT课件主要包含了高考化学一轮复习策略,电子守恒法计算,归纳整合,专项突破,真题演练明确考向,课时精练等内容,欢迎下载使用。
新高考化学一轮复习课件 第1章 第4讲 氧化还原反应: 这是一份新高考化学一轮复习课件 第1章 第4讲 氧化还原反应,共60页。PPT课件主要包含了高考化学一轮复习策略,氧化还原反应,真题演练明确考向,课时精练等内容,欢迎下载使用。
苏教版高考化学一轮复习2化学反应第5讲氧化还原反应方程式的配平及计算课件: 这是一份苏教版高考化学一轮复习2化学反应第5讲氧化还原反应方程式的配平及计算课件,共55页。












