



中考化学专题复习—离子共存问题
展开1、谁能准确叙述复分解反应发生的条件?
2、谁能准确背诵酸、碱、盐溶解性表?
3、谁能快速找出下列物质中常温下不溶于水的物质
Na2CO3 AI(OH)3 Ba(NO3)2AgCI Ba(OH)2 NH4CI BaSO4
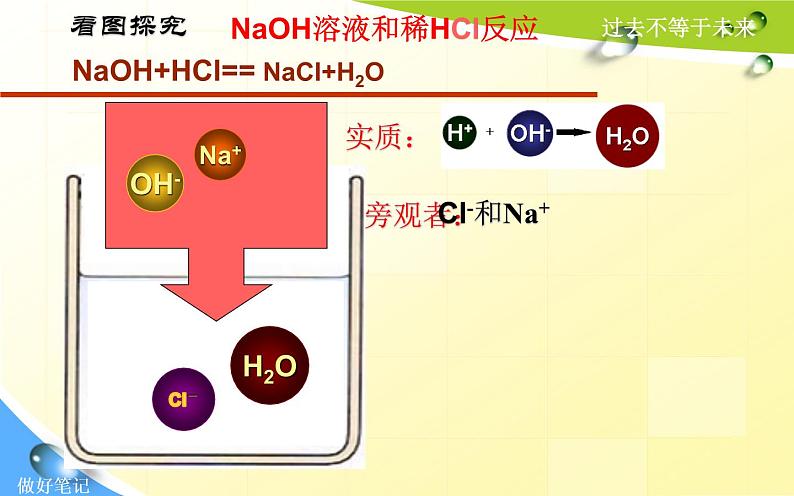
NaOH溶液和稀HCl反应
NaOH+HCl== NaCl+H2O
一、复分解反应发生的实质:
是离子之间发生反应生成气体、沉淀或水的过程。(而不发生反应的离子能共存于溶液中)
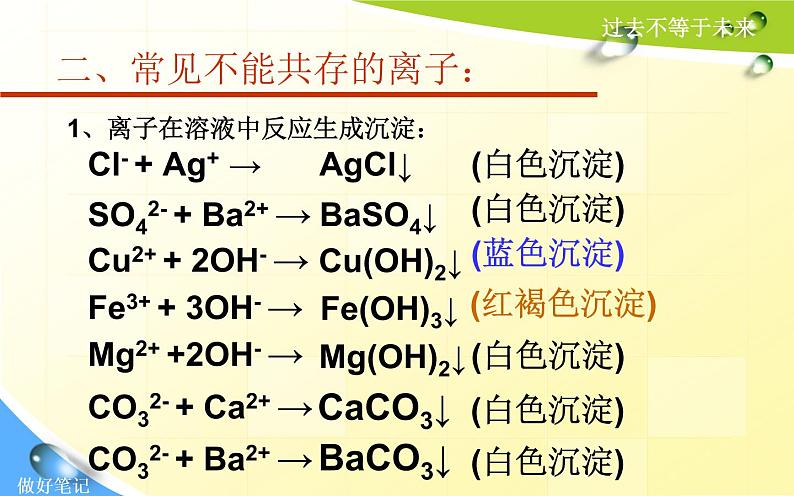
二、常见不能共存的离子:
1、离子在溶液中反应生成沉淀:
Cl- + Ag+ →
SO42- + Ba2+ →
Cu2+ + 2OH- →
Fe3+ + 3OH- →
Mg2+ +2OH- →
CO32- + Ca2+ →
CO32- + Ba2+ →
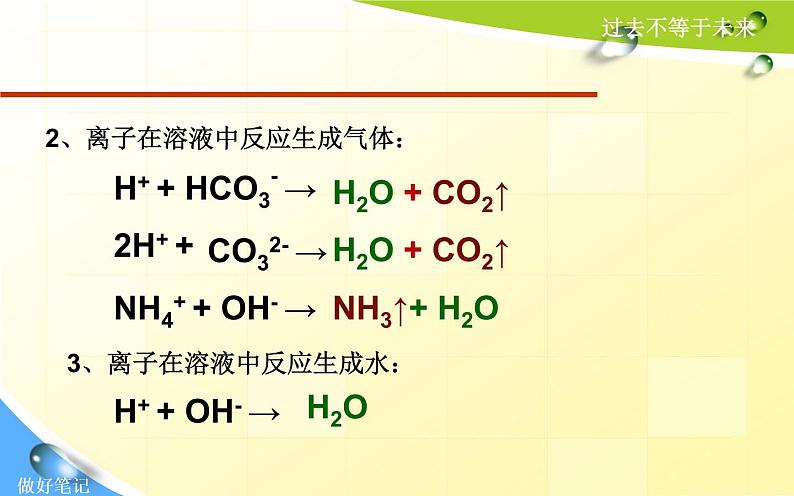
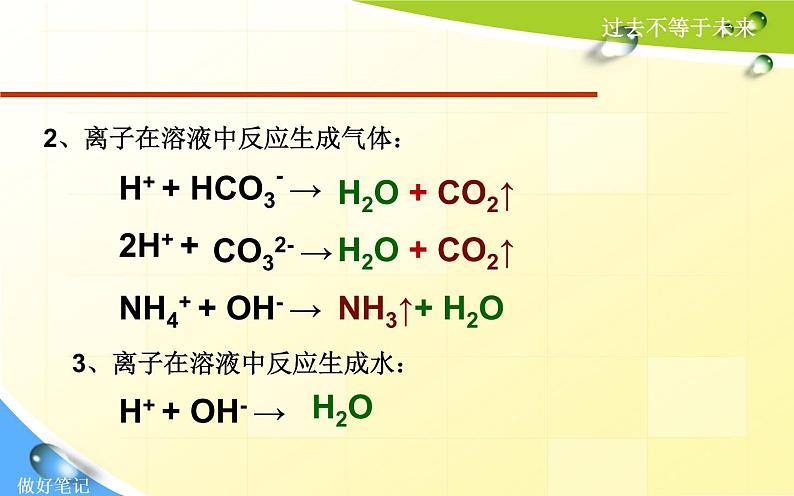
H+ + HCO3- →
H2O + CO2↑
NH4+ + OH- →
3、离子在溶液中反应生成水:
2、离子在溶液中反应生成气体:
2、离子在溶液中反应生成气体:
下列各组离子能共存的是( ) A、Ba2+ K+ H+ NO3- CO32- B、K+ Mg2+ H+ CI- NO3- C、Na+ Cu2+ Fe3+ SO42- OH- D、Ag+ Ba2+ K+ CI- NO3-
例:下列离子组能在PH=1的无色溶液大量共存的是( ) A、NO3- Fe3+ Na+ Ba2+ B、K+ SO42- Na+ NO3- C、Cl- K+ SO42- OH- D、K+ Cl- CO32- Na+
讨论:解答离子共存问题时一般步骤是哪些?
附加隐含条件的应用规律
1.溶液无色透明时,则溶液中肯定没有有色离子。 常见的有色离子是: 2.酸性溶液 中隐含存在H+。 3.碱性溶液中 中隐含存在OH-。
Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄色)
在碱性溶液中,下列各组离子能共存的是( )Na+ Cu2+ SO42- CI- Na+ H+ Fe3+ CI-K+ AI3+ NH4+ NO3-Na+ Ba2+ CI- NO3-
判断下列各组物质间能否发生反应,若能请写出反应的离子方程式。
下列各组物质,能在pH= 1的溶液中大量共存,且形成无色溶液的是( ) A.NaNO3 HCI Na2SO4 B.NaNO3 NaCI CuSO4 C.NaCI Na2SO4 Na2CO3 D.NaOH FeCI2 Na2SO4
下列各物质能在溶液中共存的是( )A.HCl、Na2SO4、Ba(OH)2 B. Ba(NO3)2、KCl、K2CO3C.NaCl、ZnSO4、KNO3 D.CuSO4、NaOH、Na2SO4
某河道两旁,有甲、乙两个工厂,它们所排放的工业废水中共含有六种离子:K+、 Ag+、 Fe3+、 CI-、 NO3-、 OH-的三种(Ag+与OH-不能共存) ,其中甲厂的废水显碱性,故甲厂废水中所含的三种离子是:_____________;乙厂废水中所含的三种离子是:________________。
K+、 CI-、 OH-
Ag+、 Fe3+、NO3-
某校初中化课外活动兴趣小组的学生,将一些可溶性化合物溶于水,配成甲、乙两瓶溶液,共含有H+、K+、Ag+、Ba2+、OH-、Cl-、CO32-、NO3-八种离子,每瓶溶液里含有四种离子各不相同。已知向甲瓶溶液中滴入紫色石蕊试液后,溶液变成红色,据此推知乙瓶溶液中的离子应该是____________________ (填离子符号)
OH-、Cl-、CO32- K+
人教版中考化学复习重难突破12物质(或离子)的共存练习课件: 这是一份人教版中考化学复习重难突破12物质(或离子)的共存练习课件,共12页。PPT课件主要包含了OH-,Cu2+,Fe2+,Fe3+等内容,欢迎下载使用。
人教版中考化学复习重难突破11物质(或离子)的共存练习课件: 这是一份人教版中考化学复习重难突破11物质(或离子)的共存练习课件,共12页。PPT课件主要包含了OH-,Cu2+,Fe2+,Fe3+等内容,欢迎下载使用。
中考化学复习重难突破11物质(或离子)的共存练习课件: 这是一份中考化学复习重难突破11物质(或离子)的共存练习课件,共12页。PPT课件主要包含了OH-,Cu2+,Fe2+,Fe3+等内容,欢迎下载使用。












