

河南省郑州市中牟县2020-2021学年高二下学期期中考试化学试题(word版 含答案)
展开河南省郑州市中牟县2020-2021学年高二下学期期中考试化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列说法正确的是
A.一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应
B. CCl4分子的比例模型为,其空间构型为正四面体
C.煤的液化是物理变化
D.检验蔗糖水解产物是否具有还原性,在水解后的溶液中,先加氢氧化钠溶液中和至碱性,再加入新制的氢氧化铜悬浊液,并加热
2.下列说法不正确的是
A.的名称为2一甲基丁烷
B.和为同一物质
C.和互为同系物
D.H2NCH2COOCH3和CH3CH2CH2NO2是同分异构体
3.关于三种有机物叙述错误的是(的性质类似于)( )
甲:阿司匹林乙:青霉素氨基酸丙:麻黄碱
A.三种有机物能发生酯化反应 B.都能与NaOH反应
C.甲的苯环上的一氯代物有4种 D.丙的分子式为C10H15ON,苯环上的一氯代物有3种
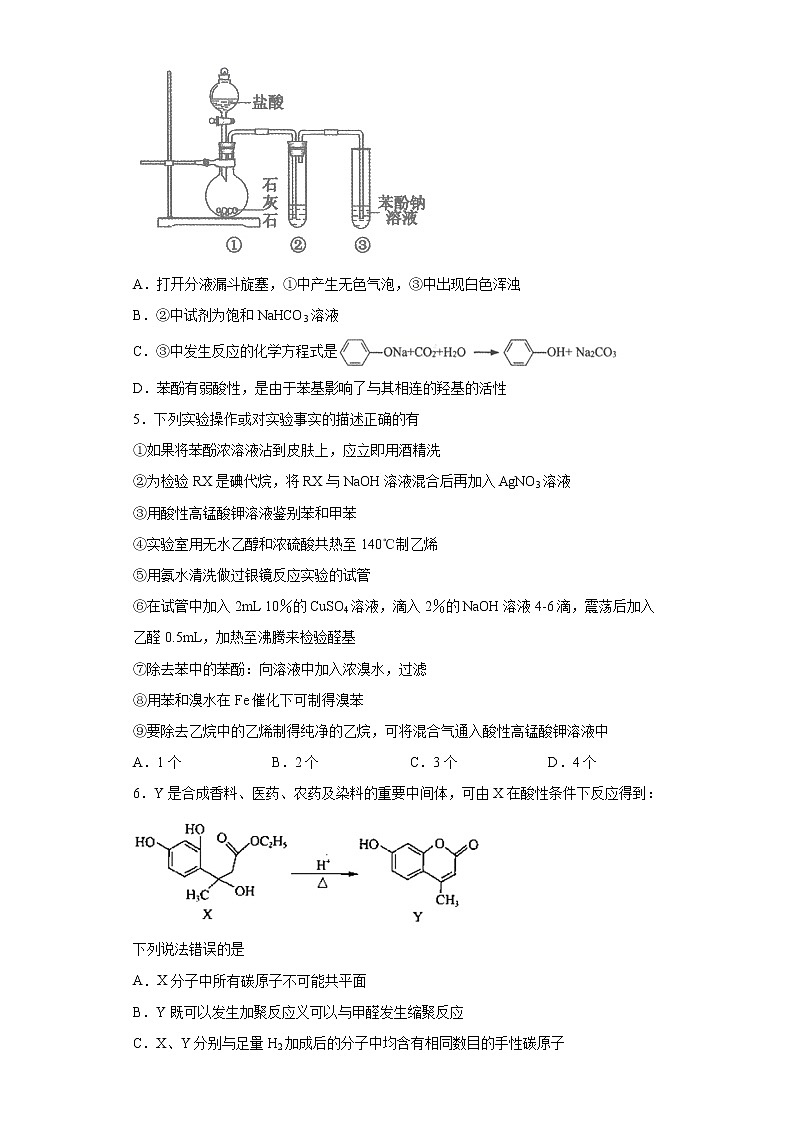
4.用如下图所示装置探究碳酸和苯酚的酸性强弱,下列叙述不正确的是(部分夹持仪器省略)
A.打开分液漏斗旋塞,①中产生无色气泡,③中出现白色浑浊
B.②中试剂为饱和NaHCO3溶液
C.③中发生反应的化学方程式是
D.苯酚有弱酸性,是由于苯基影响了与其相连的羟基的活性
5.下列实验操作或对实验事实的描述正确的有
①如果将苯酚浓溶液沾到皮肤上,应立即用酒精洗
②为检验RX是碘代烷,将RX与NaOH溶液混合后再加入AgNO3溶液
③用酸性高锰酸钾溶液鉴别苯和甲苯
④实验室用无水乙醇和浓硫酸共热至140℃制乙烯
⑤用氨水清洗做过银镜反应实验的试管
⑥在试管中加入2mL 10%的CuSO4溶液,滴入2%的NaOH溶液4-6滴,震荡后加入乙醛0.5mL,加热至沸腾来检验醛基
⑦除去苯中的苯酚:向溶液中加入浓溴水,过滤
⑧用苯和溴水在Fe催化下可制得溴苯
⑨要除去乙烷中的乙烯制得纯净的乙烷,可将混合气通入酸性高锰酸钾溶液中
A.1个 B.2个 C.3个 D.4个
6.Y是合成香料、医药、农药及染料的重要中间体,可由X在酸性条件下反应得到:
下列说法错误的是
A.X分子中所有碳原子不可能共平面
B.Y既可以发生加聚反应义可以与甲醛发生缩聚反应
C.X、Y分别与足量H2加成后的分子中均含有相同数目的手性碳原子
D.等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为4:3
7.有机物甲的结构简式为:,它可以通过下列路线合成(分离方法和其他产物已经略去):
下列说法不正确的是
A.甲可以发生取代反应、加成反应和缩聚反应
B.步骤I的反应方程式是:
C.步骤IV的反应类型是取代反应
D.步骤I和IV在合成甲过程中的目的是保护氨基不被氧化
8.下列说法正确的是
A.分子式为C4H8O2的同分异构体中,属于酸类和酯类的共有5种
B.将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成
C.除去苯中混入的少量甲苯可加入适量的酸性KMnO4溶液,充分反应后再加入足量的NaOH溶液,然后分液即可
D.等质量的苯、乙烷、乙烯和甲烷分别在氧气中充分燃烧,所消耗的氧气的量依次增加
9.阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤] 是抗非典型肺炎(SARS)的指定药物之一,其结构如右所示,有关阿昔洛韦的结构及性质的叙述中正确的是
①分子中最多有12个原子在同一平面内; ②属于芳香族化合物; ③是一种易溶于水的有机物; ④可以被氧化;⑤可以水解; ⑥可以燃烧; ⑦ 1 mol阿昔洛韦在催化剂作用下, 最多可与5molH2发生加成反应; ⑧分子式是C8H11N5O3
A.①②③④⑥⑧ B.②④⑤⑥ C.③④⑤⑥⑧ D.④⑥⑧
10.下列说法正确的是
A.可用酸性K2Cr2O7溶液检验是否酒后驾车,该应用利用了乙醇的氧化性和低沸点的性质
B.配制银氨溶液:在稀的AgNO3溶液中滴加稀氨水至恰好完全沉淀为止
C.的一溴代物和的一溴代物都有4种(不考虑立体异构)
D.与都是氨基酸且互为同系物
11.使用一种试剂无法将下列物质鉴别出来的一组是
A.苯、对二甲苯、2-己烯 B.乙酸乙酯、裂化汽油、溴苯
C.乙醇、苯酚溶液、硬脂酸甘油酯 D.甲酸、乙酸、乙醛
12.已知:(注:R、R′表示烃基),属于酮类,酮不发生银镜反应。今有如下变化:A(C6H12O2)。已知C为羧酸,C、E都不发生银镜反应,则A的结构可能有
A.1种 B.2种 C.3种 D.4种
13.下列关于有机化合物的说法正确的是
A.互为同系物的两种有机物化学性质一定相似,互为同分异构体的两种有机物化学性质一定不相似
B.与互为同分异构体,且苯环上的的一氯代物只有1种,这样的有机物共有7种
C.有机物在一定条件下可发生加成反应、聚合反应、水解反应和氧化反应
D.某羧酸酯的分子式为,该酯完全水解可得到甘油[]和羧酸,则该羧酸的分子式为
14.用下列实验装置进行相应的实验,能够达到实验目的的是( )
A.实验室制取少量硝基苯 B.证明溴乙烷、NaOH、乙醇溶液共热生成乙烯
C.分离乙酸乙酯、碳酸钠和水的混合物 D.证明乙醇浓硫酸共热生成乙烯
15.乙基香草醛是一种广泛使用的可食用香料。与乙基香草醛互为同分异构体,遇FeCl3溶液显紫色,且苯环上只有两个侧链的酯类的同分异构体有
A.6种 B.15种 C.18种 D.21种
16.实验室用下图装置完成表中的四个实验,不能达到实验目的的是
实验装置
实验目的
试剂X
试剂Y
A.
检验C2H5Br消去反应后的气体产物
水
酸性KMnO4溶液
B.
检验C2H5OH消去反应后的气体产物
NaOH溶液
Br2的CCl4溶液
C.
比较醋酸、碳酸、苯酚酸性强弱
NaOH溶液
苯酚钠溶液
D.
检验制取乙炔时的气体产物
CuSO4溶液
酸性KMnO4溶液
A.A B.B C.C D.D
二、填空题
17.按要求回答下列问题:
(1)用系统命名法命名有机物_______;
(2)相对分子质量为72且一氯代物只有一种的烷烃的结构简式_______;
(3)分子式为C5H10O2,且能与饱和NaHCO3溶液反应放出气体的有机物(不含立体异构)有_______种。
(4)分子式为C5H10且核磁共振氢谱中只有一个峰的烃的结构简式_______;
(5)乙醛与银氨溶液反应化学方程式:_______。
18.按要求回答下列问题:
(1)分子式为的有机物,有两种同分异构体,乙醇()、甲醚(),则通过下列方法,不可能将二者区别开来的是_______;
A.红外光谱B.核磁共振氢谱C.元素分析仪D.与钠反应
(2)下列实验事实不能用基团间相互作用来解释的是_______。
A.与反应时,乙醇的反应速率比水慢
B.乙醇能使重铬酸钾溶液变色而乙酸不能
C.苯酚能与溶液反应而乙醇不能
D.甲苯能使酸性溶液褪色而乙烷不能
(3)有8种物质:A乙烷;B乙烯;C乙炔;D苯;E甲苯;F溴乙烷;G聚丙烯;H环己烯。其中既不能使酸性溶液褪色,也不能与溴水反应使溴水褪色的是_______;
(4)在一定条件下能生成高分子化合物的化学方程式为_______。
(5)丁腈橡胶的结构简式为:,形成该像胶的单体为_______、_______。
(6)化合物有多种同分异构体,同时符合下列条件的同分异构体共有_______种,
①氰基()接在苯环 ②能与金属钠反应
写出其中一种核磁共振氢谱峰的面积比为的同分异构体的结构简式:_______。
三、有机推断题
19.有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤
解释或实验结论
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍
通过计算填空:(1)A的相对分子质量为:________
(2)将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g
(2)A的分子式为:________
(3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 LCO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况)
(3)用结构简式表示A中含有的官能团:__________、________
(4)A的1H核磁共振谱如图
(4)A中含有________种氢原子
(5)综上所述,A的结构简式________
20.洛索洛芬钠可用于缓解类风湿性关节炎、肩周炎等炎症。化合物Ⅰ是合成该药物的一种中间体,合成Ⅰ的路线如图。回答下列问题:
已知:①
②RBr
③
(1)A的名称为_______,C中含有官能团的名称为_______。
(2)的反应类型为_______,G的结构简式为_______。
(3)检验A是否完全转化为B的试剂为_______。
(4)的化学方程式为_______,的化学方程式为_______。
(5)符合下列条件的D的同分异构体有_____种,写出其中核磁共振氢谱有4组峰,峰面积之比为的化合物的结构简式_______。
①属于芳香族化合物 ②能发生水解反应和银镜反应
(6)参照图中流程,设计由2-溴丁烷和乙酸乙酯为原料制备的合成路线其他试剂任选)_______。
四、实验题
21.某化学小组采用如图装置,以环己醇制备环己烯:
密度(g/cm3)
熔点(℃)
沸点(℃)
溶解性
环己醇
0.96
25
161
能溶于水
环己烯
0.81
-103
83
难溶于水
已知:
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,
在试管C内得到环己烯粗品。
①试管C置于冰水浴中的目的是 _____________________________________。
②导管B除了导气外还具有的作用是____________,A中碎瓷片的作用是 ___________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______ 层(填“上”或“下”),分液后用___________________(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按图装置蒸馏,冷却水从________口进入。蒸馏时要加入生石灰,目的是:_________________________。
③收集产品时,控制的温度应在________________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 _______
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_______
A.用酸性高锰酸钾溶液 B.用金属钠 C.测定沸点
参考答案
1.D
【详解】
A.葡萄糖是单糖,不能发生水解反应,A错误;
B.CCl4分子是正四面体结构,但由于Cl原子半径比C大,因此该图示不是CCl4的比例模型,B错误;
C.煤的液化过程有新物质产生,因此发生的变化为化学变化,C错误;
D.蔗糖水解需要稀硫酸作催化剂,检验蔗糖水解产物是否具有还原性,应该先在水解后的溶液中加氢氧化钠溶液中和催化剂硫酸,使溶液呈碱性,然后再加入新制的氢氧化铜悬浊液,并加热煮沸,若产生砖红色沉淀,证明产生了葡萄糖,说明蔗糖水解产物是否具有还原性, D正确;
故合理选项是D。
2.C
【详解】
A.根据系统命名法,该烷烃主链有4个碳原子,第2个碳原子上有一个甲基,命名为2—甲基丁烷,A正确;
B.由于甲烷为正四面体结构,则和为同一物质,B正确;
C. 互为同系物的物质必须结构相似,的结构中羟基连在苯环上,为酚类物质,的结构中羟基连在-CH2-上,为醇类物质,二者不互为同系物,C错误;
D. H2NCH2COOCH3和CH3CH2CH2NO2的分子式相同,结构不同,二者互为同分异构体,D正确;
答案选C。
【点睛】
C项为易错点,注意酚类物质和醇类物质结构的区别。
3.B
【详解】
A.三种有机物分别含有羧基、、羟基,都可发生酯化反应,故A正确;
B.阿司匹林含有羧基和酯基,青霉素氨基酸含有羧基,它们都可与氢氧化钠反应,麻黄碱不含羧基,也不含酚羟基,它不能用与氢氧化钠反应,故B错误;
C. ,苯环上有4种等效氢,苯环上的一氯代物有4种,故C正确;
D. 麻黄碱的分子式为C10H15ON,苯环上有3种等效氢,苯环上的一氯代物有3种,故D正确;
选B。
【点睛】
本题考查有机物的结构和性质,侧重于学生的分析能力的考查,本题注意把握有机物官能团的性质,特别是羧基、羟基的性质,学会用等效氢法判断同分异构体的数目。
4.C
【详解】
A.装置①中碳酸钙与盐酸反应生成二氧化碳气体,所以打开分液漏斗旋塞,①中产生无色气泡;装置③中二氧化碳与苯酚钠溶液反应生成苯酚,苯酚不溶于冷水,则③中出现白色浑浊,故不选A;
B.实验①中碳酸钙与盐酸反应生成二氧化碳气体,由于盐酸具有挥发性,则制取的二氧化碳气体中混有杂质氯化氢,氯化氢能够与苯酚钠溶液反应,影响实验结果,所以需要用②中饱和碳酸氢钠溶液除去氯化氢,故不选B;
C.苯酚酸性大于碳酸氢根离子,苯酚钠溶液与二氧化碳反应生成苯酚和碳酸氢钠,反应的化学方程式为:C6H5ONa+CO2+H2O=C6H5OH+NaHCO3,故选C;
D.结构决定性质,如:受苯基的影响,与苯基相连的羟基变得比较活泼,导致苯酚具有弱酸性,故不选D;
答案:C
【点睛】
利用强酸制弱酸原理来判断酸性强弱,注意①盐酸易挥发,要防干扰②H2CO3>C6H5OH>HCO3-。
5.B
【详解】
①苯酚和酒精都是有机物,苯酚易溶于酒精,苯酚浓溶液沾到皮肤上,应立即用酒精洗,故①正确;
②向RX中加入NaOH溶液充分反应后,取上层清液并加入AgNO3溶液,上层清夜中的氢氧化钠和硝酸银反应,生成氢氧化银白色沉淀,该沉淀会分解生成黑色的氧化银,不可观察到有黄色沉淀生成,故②错误;
③用酸性高锰酸钾溶液鉴别苯和甲苯,甲苯被紫红色的高锰酸钾氧化成苯甲酸,高锰酸钾溶液褪色,而苯无此性质,所以能鉴别,故③正确;
④实验室用无水乙醇和浓硫酸共热至170℃制乙烯,故④错误;
⑤氨水不能和银反应,做过银镜反应实验的试管上附着单质银,所以不能用氨水洗,故③错误;
⑥检验醛基需在碱性环境下,氢氧化钠需过量,故⑥错误;
⑦除去苯中的苯酚:向苯中含有苯酚的溶液中加入浓溴水,苯酚和溴水反应生成三溴苯酚,三溴苯酚是有机物,溶于苯中,无法过滤,故⑦错误;
⑧用苯和液溴在FeBr3催化下可制得溴苯,不与溴水反应,故⑧错误;
⑨要除去乙烷中的乙烯制得纯净的乙烷,将混合气通入酸性高锰酸钾溶液中,酸性高锰酸钾将乙烯氧化成二氧化碳,二氧化碳混在乙烷中,得不到纯净的乙烷,故⑨错误;
①③正确,其余均错误。
故答案选:B。
【点睛】
苯和液溴在FeBr3催化下可制得溴苯,不与溴水反应。
6.D
【详解】
A.X中含有饱和碳原子,具有甲烷的结构特征,则所有的碳原子不可能在同一个平面上,A项正确;
B.Y含有碳碳双键,可以发生加聚,Y含有酚羟基,有酚的特点,可以和甲醛发生缩聚反应,,故B项正确;
C.X、Y分别与足量加成后生成和,均含有4个手性碳原子,C项正确;
D.X中酚羟基、酯基可与氢氧化钠溶液反应,1molX可与3 mol 氢氧化钠反应;Y中酚羟基、酚酯基可与氢氧化钠反应,且1mol酚酯能与2 mol 氢氧化钠反应,则1moY可与3 mol NaOH反应,最多消耗NaOH的物质的量之比为1:1,D项错误;
故选D。
7.B
【详解】
A. 甲分子中含有氨基、羧基和苯环,可以发生取代反应、加成反应和缩聚反应,A正确;B. 步骤I是取代反应,反应方程式是+HCl,B错误;C. 戊的结构简式为,步骤IV是戊中的肽键发生水解反应,因此反应类型是取代反应,C正确;D. 氨基易被氧化,因此步骤I和IV在合成甲过程中的目的是保护氨基不被氧化,D正确,答案选B。
8.C
【详解】
A.分子式为C4H8O2的同分异构体中,属于酸类和酯类的有CH3CH2CH2COOH、、HCOOCH2CH2CH3、、CH3COOCH2CH3、CH3CH2COOCH3,共6种,A错误;
B.电石中含有CaS、Ca2P3等杂质,将电石与水反应产生的乙炔气体中含有的H2S、PH3等杂质,也具有还原性,会被酸性KMnO4溶液氧化而使溶液褪色,因此不能据此判断是否产生乙炔气体,B错误;
C.甲苯可被酸性KMnO4溶液氧化产生,而苯不能反应,向含有甲苯的苯中加入适量的酸性KMnO4溶液充分反应后加入NaOH溶液,发生中和反应转化为可溶于水的,然后分液即可将难溶于水的苯分离出来,C正确;
D.苯、乙烷、乙烯和甲烷分子式分别是C6H6、C2H6、C2H4、CH4,12 g C完全燃烧消耗1 mol O2,4 g H完全燃烧消耗1 mol O2,可见当物质质量相等时,H元素含量越大,完全燃烧消耗O2质量越大。C2H6中H的含量比C2H4大,因此当物质质量相等时C2H6消耗O2比C2H4多,D错误;
故合理选项是C。
9.C
【详解】
①分子中最多有13个原子在同一平面内,①不正确;②其分子中不含苯环,所以不属于芳香族化合物,②不正确;③其分子中有多个亲水基,可以与水分子间形成氢键,所以其是一种易溶于水的有机物,③正确;④分子中有氨基、羟基、碳碳双键等都可以被氧化,④正确;⑤分子中有酰胺键,可以水解,⑤正确;⑥有机物一般均可以燃烧,⑥正确;⑦ 1 mol阿昔洛韦在催化剂作用下,最多可与4molH2发生加成反应,⑦不正确;⑧分子式是C8H11N5O3,⑧正确。综上所述,C正确,本题选C。
10.C
【详解】
A.乙醇易挥发具有还原性,酸性K2Cr2O7溶液具有强氧化性,K2Cr2O7会将乙醇氧化,其本身被还原为绿色Cr3+,常利用这一性质检验司机是否酒后驾车,A错误;
B.在稀的AgNO3溶液中滴加稀氨水,二者反应产生AgOH白色沉淀,当氨水过量时,AgOH与过量氨水反应产生可溶性的Ag(NH3)2OH,即产生银氨溶液,当滴加至最初产生的沉淀恰好溶解时得到的溶液就是银氨溶液,B错误;
C.在苯环上有三种不同位置的H原子,在侧链-CH3有一种H原子,因此该物质分子中含有四种不同位置的H原子,故其一溴代物有4种;分子中含有四种不同位置的H原子,故其一溴代物也有4种,C正确;
D.与分子中的氨基与羧基连接在同一个C原子上,属于氨基酸,但二者在分子组成上相差1个CH2原子团,但前者有2个酚羟基,后者只有1个酚羟基,结构不相似,因此二者不是同系物,D错误;
故合理选项是C。
11.A
【详解】
A、对二甲苯、2-己烯、苯都不溶于水,对二甲苯和2-己烯都能使酸性高锰酸钾溶液褪色,己烯可使溴水褪色,用一种试剂不能鉴别,选项A错误;
B、在乙酸乙酯、裂化汽油、溴苯中分别加入溴水,乙酸乙酯、溴苯与溴水不反应,但溶液分层,乙酸乙酯的密度比水小在上层,溴苯的密度比水大在下层,裂化汽油与溴水发生加成反应而使其褪色,现象各不相同,可鉴别,选项B正确;
C、乙醇、苯酚溶液、硬脂酸甘油酯分别加入溴水,乙醇和硬脂酸甘油酯均不反应,但前者互溶后者不互溶而分层,苯酚与溴反应生成白色沉淀三溴苯酚,现象不同,能用一种物质鉴别,选项C正确;
D、加入新制的Cu(OH)2悬浊液,乙醛在加热条件下发生反应生成砖红色沉淀,甲酸溶解新制的Cu(OH)2悬浊液,加热条件下反应生成砖红色沉淀,乙酸与新制的Cu(OH)2悬浊液发生中和反应,加热无明显现象,现象不同,可鉴别,选项D正确;
答案选A。
【点睛】
本题考查有机物的鉴别,为高频考点,把握常见有机物的性质及性质差异为解答的关键,侧重氧化、加成反应及萃取的考查,题中涉及物质都为烃,只用一种物质就可鉴别,则可根据物质的密度大小以及烯烃与溴水发生加成反应的性质解答。
12.B
【详解】
A的分子式为C6H12O2,A在碱性条件下反应生成B和D,B与酸反应,B应为盐,D能在Cu催化作用下发生氧化,D应为醇,则A属于酯,C和E都不能发生银镜反应,说明C、E不含醛基,则C不可能为甲酸,若C为乙酸,则D为CH3CH(OH)CH2CH3,若C为丙酸,则D为CH3CH(OH)CH3,若C为丁酸,则D为乙醇、E为乙醛,不可能,所以A只能为:CH3COOCH(CH3)CH2CH3或CH3CH2COO2CH(CH3)2,总共有两种可能的结构,故选B。
13.B
【详解】
A.互为同系物的两种有机物结构相似,因此二者的化学性质一定相似;互为同分异构体的两种有机物结构不一定相似,如丙烯与环丙烷是同分异构体,前者为烯烃,分子中含有碳碳双键,能够发生加成反应;后者分子中存在碳碳单键,特征反应是取代反应,因此二者的化学性质不一定相似,A错误;
B.与互为同分异构体,且苯环上的的一氯代物只有1种,说明该物质分子高度对称,苯环上只有一种位置的H原子,该物质可能的结构为、、、、、、7种结构,B正确;
C.该有机物含有碳碳双键,可发生加成反应、加聚反应;分子中无酯基,不能发生水解反应,C错误;
D.酯水解过程中产生的高级脂肪酸分子中含有C原子数为,含有的H原子数为:,含有的O原子数为:,所以该羧酸的分子式为C18H34O2,D错误;
故合理选项是B。
14.D
【详解】
A.制备硝基苯应水浴加热,温度计测定水温度,加热至50℃~60℃,A错误;
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化,所以酸性高锰酸钾溶液褪色不能说明乙烯的生成,B错误;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层,则利用分液法分离,不能利用过滤分离,C错误;
D.乙醇和浓硫酸混合加热到170℃发生消去反应生成乙烯,过程中副反应为浓硫酸脱水性得到碳和浓硫酸加热反应生成二氧化碳和二氧化硫,二氧化硫具有还原性和溴单质发生反应,检验乙烯前需要除去二氧化硫,装置中乙烯发生装置正确,通过氢氧化钠溶液吸收生成的二氧化硫和二氧化碳,剩余气体通过溴的四氯化碳溶液褪色证明生成乙烯,实验装置能够达到实验目的,D正确;
答案选D。
15.C
【详解】
遇FeCl3溶液显紫色,说明有酚羟基;苯环上只有两个侧链的酯类,则另一个取代基可以是-OOCCH2CH3、-CH2OOCCH3、-CH2CH2OOCH、-CH(CH3)OOCH、-COOCH2CH3、-CH2COOCH3,苯环上有2个取代基,有邻间对三种结构,则共有3×6=18种,C符合题意;
答案选C。
16.C
【详解】
A. C2H5Br发生消去反应生成乙烯和溴化氢,乙烯和溴化氢均能使酸性高锰酸钾溶液褪色,为防止溴化氢对乙烯的干扰,试剂X可除去溴化氢,因此可达到实验目的,A项正确;
B. 乙醇发生消去反应生成乙烯,反应过程中浓硫酸可能会与有机物反应生成SO2,生成的SO2会和溴反应,将干扰实验结果,所以用X溶液吸收可能产生的SO2,用Y溶液检验乙烯,表格中所列试剂能实现实验目的,B项正确;
C. 醋酸具有挥发性,生成的二氧化碳中含有乙酸,试剂X是为了除去挥发的醋酸,但氢氧化钠不仅可以与醋酸反应,还可以与生成的二氧化碳反应,不满足除杂原则,不能达到实验目的,C项错误;
D. 电石和食盐水反应生成乙炔,同时还生成杂质气体硫化氢等,硫化氢能和硫酸铜反应生成CuS沉淀,且硫化氢、乙炔都能被酸性高锰酸钾溶液氧化,X能除去硫化氢气体,防止乙炔的检验,Y能检验乙炔,能实现实验目的,D项正确;
答案选C。
17.2,2,4三甲基己烷 4 CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O
【详解】
(1)物质的分子中最长碳链上含有6个C原子,从离支链较近的左端为起点,给主链上C原子编号,以确定支链的位置,该物质名称为2,2,4三甲基己烷;
(2)假设烷烃分子式为CnH2n+2,该烷烃的相对分子质量为72,则14n+2=72,则n=5,分子式是C5H12,其一氯代物只有一种,说明该物质分子中只有一种位置的H原子,其结构简式是;
(3)分子式为C5H10O2,且能与饱和NaHCO3溶液反应放出气体的有机物是饱和一元羧酸,其同分异构体(不含立体异构)有CH3CH2CH2CH2COOH、、、,共4种不同结构;
(4)某烃分子式为C5H10且核磁共振氢谱中只有一个峰,说明该烃分子中只有一种H原子,该烃为环戊烷,其结构简式为;
(5)乙醛分子中含有醛基,能够被银氨溶液氧化产生CH3COOH,CH3COOH与氨反应产生CH3COONH4,银氨溶液被还原产生Ag单质,该反应的化学方程式为:CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O。
18.C B ADFG CH2=CH-CN 13
【详解】
(1) A.乙醇和甲醚含化学键、官能团不同,则红外光谱可区分二者,故A不符合题意;
B.乙醇含3种H,甲醚含1种H,则可以用核磁共振谱区分二者,故B不符合题意;
C.乙醇和甲醚的分子式相同,各元素的比重相同,则不能使用元素分析仪区分这两种物质,故C符合题意;
D.乙醇与钠反应生成氢气,而甲醚不能,则可用这个方法区分二者,故D不符合题意;
故选C;
(2) A.乙醇中羟基不如水中羟基活泼,说明烃基对羟基产生影响,A不符合题意;
B.乙醇具有还原性,乙酸不具有还原性,这是官能团的性质,与所连基团无关,B符合题意;
C.苯酚可以看作是苯环和羟基连接,乙醇可以可作是乙基和羟基连接,苯酚能跟NaOH溶液反应而乙醇不能,则说明苯基对羟基有影响,C不符合题意;
D.甲苯可以看作是甲基和苯环连接,乙烷可以看成是甲基和甲基连接,甲苯能使KMnO4酸性溶液褪色,说明苯环对甲基有影响,D不符合题意;
故选B;
(3) A.乙烷既不能使酸性高锰酸钾溶液褪色,也不能与溴水反应,A符合题意;
B.乙烯含碳碳双键,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使溴水褪色,B不符合题意;
C.乙炔含碳碳叁键,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使溴水褪色,C不符合题意;
D.苯的化学性质稳定,既不能使酸性高锰酸钾溶液褪色,也不能与溴水反应,D符合题意;
E.甲苯能使使酸性高锰酸钾溶液褪色,但不能与与溴水反应,E不符合题意;
F.溴乙烷既不能使酸性高锰酸钾溶液褪色,也不能与溴水反应,F符合题意;
G.聚丙烯不含不饱和键,既不能使酸性高锰酸钾溶液褪色,也不能与溴水反应,G符合题意;
H.环己烯含有碳碳双键,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使溴水褪色,H不符合题意;
综上所述,符合题意的有ADFG,故选ADFG;
(4) 含有碳碳双键,在一定条件下,其生成高分子化合物的化学方程式为;
(5)丁腈橡胶的单体为、;
(6)能与金属钠反应,说明该物质含有羟基;氰基接在苯环上,若苯环上的另一个取代基为-CH2OH,该物质的同分异构体有3种;若苯环上除了有氰基,还有羟基和甲基,则有以下三种情况:①氰基和羟基处于对位,该物质的同分异构体有2种;②氰基和羟基处于间位,该物质的同分异构体有4种;③氰基和羟基处于邻位,该物质的同分异构体有4种;综上所述,符合条件的同分异构体有13种;其中一种核磁共振氢谱峰的面积比为1:2:2:2的同分异构体的结构简式为。
19.90 C3H6O3 -COOH -OH 4 CH3CH(OH)COOH
【分析】
(1)有机物和氢气的密度之比等于相对分子质量之比;
(2)浓硫酸可以吸收水,碱石灰可以吸收二氧化碳,根据元素守恒来确定有机物的分子式;
(3)羧基可以和碳酸氢钠发生化学反应生成二氧化碳,羟基可以和金属钠发生化学反应生成氢气;
(4)核磁共振氢谱图中有几个峰值则含有几种类型的等效氢原子,峰面积之比等于氢原子的数目之比;
(5)根据分析确定A的结构简式。
【详解】
(1)有机物质的密度是相同条件下H2的45倍,所以有机物的相对分子质量为45×2=90,故答案为90;
(2)浓硫酸增重5.4g,则生成水的质量是5.4g,生成水的物质的量是=0.3mol,所含有氢原子的物质的量是0.6mol,碱石灰增重13.2g,所以生成二氧化碳的质量是13.2g,所以生成二氧化碳的物质的量是 = 0.3 mol,所以碳原子的物质的量是0.3 mol,由于有机物是0.1mol,所以有机物中碳原子个数是3,氢原子个数是6,根据相对分子质量是90,所以氧原子个数是3,即分子式为:C3H6O3,
故答案为C3H6O3;
(3)只有羧基可以和碳酸氢钠发生化学反应生成二氧化碳,生成2.24LCO2(标准状况),则含有一个羧基(-COOH),醇羟基(-OH)可以和金属钠发生反应生成氢气,与足量金属钠反应生成2.24LH2(标准状况),则含有羟基数目是1个,
故答案为-COOH和-OH;
(4)根据核磁共振氢谱图看出有机物中有4个峰值,则含4种类型的等效氢原子,氢原子的个数比是3:1:1:1,
故答案为4;
(5)综上所述,A的结构简式为CH3CH(OH)COOH。
20.苯甲醛 溴原子 取代反应 新制的氢氧化铜或银氨溶液 +HBr(浓)→+H2O +CH3OH+H2O 14
【分析】
结合已知②RBr,根据逆推法,由D()反推出C为,B应该为,与HBr发生取代反应生成和水,结合已知:①可知,A为苯甲醛,反应后酸化得到B为;与甲醇在浓硫酸催化下发生酯化反应生成E为,在甲醛和溴化氢及催化剂作用下反应生成F为;由已知③可知,G反应生成H为,可推知G为;与反应生成I为。
【详解】
(1) A为苯甲醛;C为,含有官能团的名称为溴原子;
(2)是与反应生成和溴化氢,反应类型为取代反应,G的结构简式为;
(3)A为苯甲醛,检验A是否完全转化为B(),即不再含有醛基,所需要的试剂为新制的氢氧化铜或银氨溶液;
(4)的化学方程式为+HBr(浓)→+H2O,的化学方程式为+CH3OH+H2O;
(5) D()的同分异构体①属于芳香族化合物;②能发生水解反应和银镜反应,则含有甲酸酯的结构,若苯环上只有一个取代基,取代基可以是HCOOCH2CH2-、HCOOCH(CH3)-共2种;若苯环上有二个取代基,可以为HCOOCH2-和甲基,位置上有邻、间、对位,则有3种;可以为HCOO-和乙基,位置上有邻、间、对位,则有3种;若苯环上有三个取代基,则二个甲基和一个HCOO-,以两个甲基在邻、间、对位上,然后HCOO-放上去分别有2种、3种、1种共6种;故总共有14种;其中核磁共振氢谱有4组峰,峰面积之比为的化合物,则含有2个甲基且高度对称,符合条件的结构简式为、;
(6)参照图中流程,乙酸乙酯在醇钠和酸作用下生成,与2-溴丁烷在一定条件下反应生成,合成路线如下:。
21.防止环己烯挥发 冷凝 防暴沸 上 C g 除去水分 83ºC C BC
【分析】
环己醇在浓硫酸存在下加热到85℃生成环己烯,应采用水浴加热,长导管可以起导气和冷凝的作用;分离环己烯中的环己醇和酸性杂质,需要进行分液,然后用碳酸钠溶液洗涤,减少产品中的环己醇和酸性杂质;环己醇能和金属钠反应,但环己烯不能;二者都能和酸性高锰酸钾溶液反应。
【详解】
(1)①环己烯的沸点较低,为83℃,放在冰水浴中可以防止环己烯挥发;
②长导管有导出气体和冷凝的作用;液体中加入碎瓷片的作用是防止液体加热过程中暴沸;
(2)①环乙烯的密度比水小,在上层,分液后用碳酸钠溶液洗涤,洗去酸性杂质和环己醇等;
②冷凝装置中水流方向是下进上出,即g口进,f口出;生石灰能和水反应,所以蒸馏时加入生石灰能干燥;
③因为环己烯的沸点为83℃,所以控制的温度应在83℃左右;
A.蒸馏时从70℃开始收集产品,则产品的质量高,A错误;
B.环己醇实际用量多了,会使产品的量增加,B错误;
C.制备粗品时环己醇随产品一起蒸出,会使生成的环乙烯量减少,C正确;
故选C;
(3)环己烯粗品中含有少量的环己醇,故可以通过鉴别环己醇的存在,来鉴别环己烯的精品和粗品;
A.环己烯和环己醇都能使酸性高锰酸钾溶液褪色,故不能通过酸性高锰酸钾来鉴别环己烯的精品和粗品,A错误;
B.环己醇能与金属钠反应,但环己烯不能,可以用金属钠来鉴别环己烯的精品和粗品,B正确;
C.测定沸点的方法可以鉴别环己烯的精品和粗品,C正确;
故合理的方法为BC。
河南省郑州市中牟县2023-2024学年高一上学期期末测评化学试题(PDF版含答案): 这是一份河南省郑州市中牟县2023-2024学年高一上学期期末测评化学试题(PDF版含答案),文件包含2023-2024学年河南省郑州市中牟县高一上学期期末联考化学pdf、24高一化学上期末答案pdf等2份试卷配套教学资源,其中试卷共7页, 欢迎下载使用。
河南省郑州市中牟县2023-2024学年高二上学期期中考试化学试题: 这是一份河南省郑州市中牟县2023-2024学年高二上学期期中考试化学试题,共10页。试卷主要包含了单项选择题,选择题,填空题等内容,欢迎下载使用。
河南省郑州市民高2022-2023学年高二上学期期中考试化学试题(Word版含答案): 这是一份河南省郑州市民高2022-2023学年高二上学期期中考试化学试题(Word版含答案),共27页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












