





初中化学人教版九年级下册课题2 酸和碱的中和反应背景图ppt课件
展开1.认识酸和碱之间发生的中和反应。
3.了解中和反应在实际中的应用。
2.从微观角度初步认识中和反应发生 的原理。
1.研究酸和碱发生中和反应的过程。
2.会书写中和反应的化学方程式。
从微观角度认识中和反应的原理。
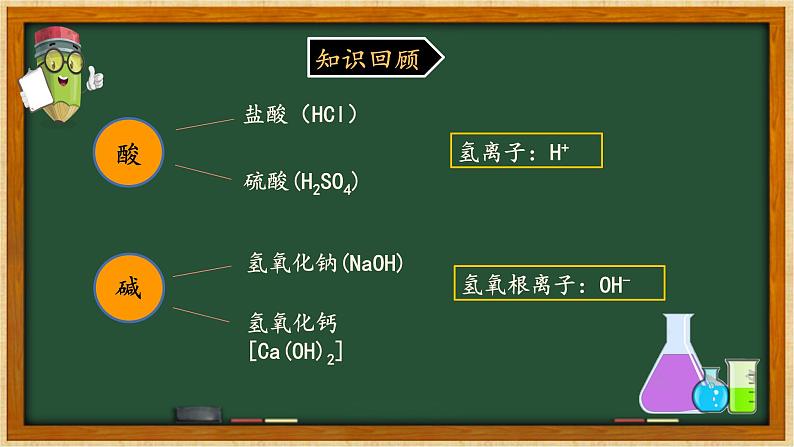
氢氧化钙[Ca(OH)2]
想一想:氢氧化钠溶液和稀盐酸到底有没有发生反应呢?
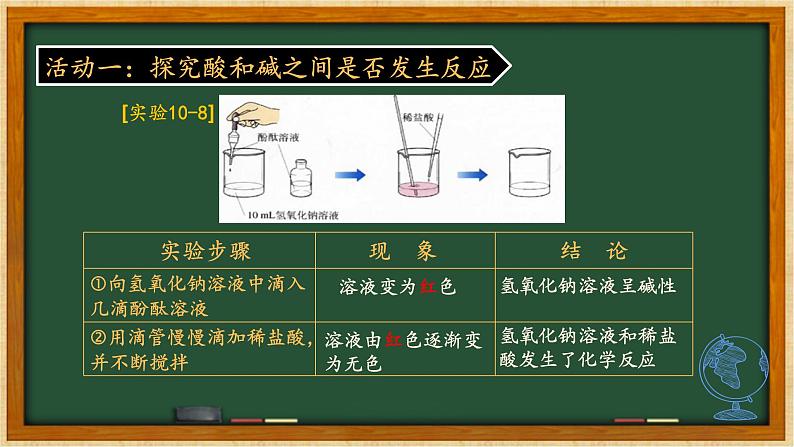
活动一:探究酸和碱之间是否发生反应
溶液由红色逐渐变为无色
氢氧化钠溶液和稀盐酸发生了化学反应
为什么酚酞溶液红色消失,就能说明氢氧化钠溶液与稀盐酸发生了反应呢?
酚酞溶液红色消失,说明烧杯中的物质已经没有氢氧化钠,因此氢氧化钠溶液与稀盐酸一定发生了反应。
提示:判断反应的发生时,不仅要依据实验现象进行判断,更需要 从化学原理上加以解释,以获得本质性的认识。
判断没有明显现象的酸和碱反应时,能否用石蕊溶液作指示剂呢?
一般情况下,酸碱反应时不选用石蕊作指示剂,原因是石蕊的红色、紫色和蓝色变化时,视觉观察不够明显。
思考:氢氧化钠溶液与稀盐酸反应后的无色溶液中 含有哪些物质呢?
3.酸和碱反应的实质:H+ + OH- = H2O
2.反应的化学方程式:HCl + NaOH = NaCl +H2O
酸中都含有氢离子(H+),碱中都含有氢氧根离子(OH-),氢离子(H+)和氢氧根离子(OH-)能结合生成水分子,因此酸和碱一定能发生化学反应。
练习:写出下列反应的化学方程式
H2SO4+2NaOH = Na2SO4+2H2O
2HCl+Ca(OH)2= CaCl2+2H2O
H2SO4+Cu(OH)2= CuSO4+2H2O
HCl + NaOH = NaCl +H2O
盐:由金属离子和酸根离子构成的化合物。
中和反应:酸与碱作用生成盐和水的反应。
盐→金属离子+酸根离子
CO2 + 2NaOH = Na2CO3 + H2O
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
以下反应均生成盐和水,它们是不是中和反应呢?
中和反应:酸+碱 →盐+水
1.阅读教材第61页相关内容,了解酸和碱的中和反应在实际生活中有哪些应用? 2.你还能举出一些常见的酸碱中和反应的实例吗?
活动三:了解中和反应的应用
调节土壤酸碱性:若土壤酸性增强,加熟石灰Ca(OH)2
处理工厂废水:印染厂废水(碱性)→ 硫酸硫酸厂污水(酸性)→ 熟石灰
治疗胃酸过多:胃酸的主要成分是盐酸,用含有氢氧化铝的药物中和过多胃酸
涂含有碱性物质的溶液减轻蚊虫叮咬的痛痒等
Ca(OH)2+H2SO4=CaSO4+2H2O
Al(OH)3+3HCl=AlCl3+3H2O
1.下列反应属于中和反应的是( ) A.Na2CO3+2HCl=2NaCl+H2O+CO2↑ B.2NaOH+H2SO4 = Na2SO4+2H2O C.SO2+2NaOH = Na2SO3+H2O D.Fe+CuSO4 = Cu+FeSO4
2.蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体射入一 种叫蚁酸(具有酸的性质)的物质,使皮肤红肿、 瘙痒甚至疼痛。要消除这种症状,可在叮咬处涂抹 下列物质中的( ) A.牙膏或肥皂水 B.食盐水 C.烧碱 D.食醋
3.如图为“胃酸完全抑制剂”的标签。“胃酸完全抑制剂”的主要成分中属于盐的物质是 (写化学式)。 (2)服用“胃酸完全抑制剂”后在胃内发生反应的化学方程式是 , 。
CaCO3+2HCl=CaCl2+H2O+CO2↑
Mg(OH)2+2HCl=MgCl2+2H2O
H+ + OH- = H2O
初中化学人教版九年级下册课题2 溶解度背景图ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度背景图ppt课件,共38页。PPT课件主要包含了实验结论,饱和溶液,不饱和溶液,降低温度,升高温度,1大多数,增加溶质,蒸发溶剂,增加溶剂等内容,欢迎下载使用。
初中化学人教版九年级下册第八单元 金属和金属材料课题 1 金属材料教案配套课件ppt: 这是一份初中化学人教版九年级下册第八单元 金属和金属材料课题 1 金属材料教案配套课件ppt,共37页。PPT课件主要包含了铜商代,铁春秋战国,铝一百多年,一些金属的物理性质,使用是否便利,废料是否易于回收,是否美观,对环境的影响,资源丰富,无毒轻便等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度图片ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度图片ppt课件,共40页。













