
四川省成都市第七中学2021届高三5月月考理综化学试卷
展开本试卷分选择题和非选择题两部分。第I卷(选择题),第II卷(非选择题)
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡规定的位置上。
2.答选择题时,必须用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦
干净后,再选涂其他答案标号。
3.答非选择题时,必修使用0.5毫米黑色签字笔,将答案写在答题卡规定的位置上。
4.所有题目必修在答题卡上作答,在试卷上答题无效。
5.考试结束后,只将答题卡交回。
第I卷
一、选择题:本题共7个小题,每小题6分。共42分,在每小题给出的四个选项中,只有一
项是符合题目要求的。
7.化学科学在“国之重器”的打造中发挥着重要作用。下列有关叙述正确的是( )
A.“墨子号”卫星成功发射实现了光纤量子通信,生产光纤的原料为晶体硅
B.嫦娥5号携带的月壤中,富含的3He与地球上的4He互为同素异形体
C.长征五号火箭的箭体蒙皮材料2219-铝合金,可一定程度上减轻火箭的质量
D.“奋斗者”号载人潜水器成功坐底,深度10909m,所用的合金潜孔钻头硬度与熔沸点均比其
单一组分高
8.能正确表示下列反应的离子方程式是( )
A.向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
B.NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-NH3↑+SO32-+2H2O
C.向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性:
H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.向KIO3与KI混合溶液中加入醋酸发生反应生成I2:IO3-+5I-+6H+=3I2+3H2O
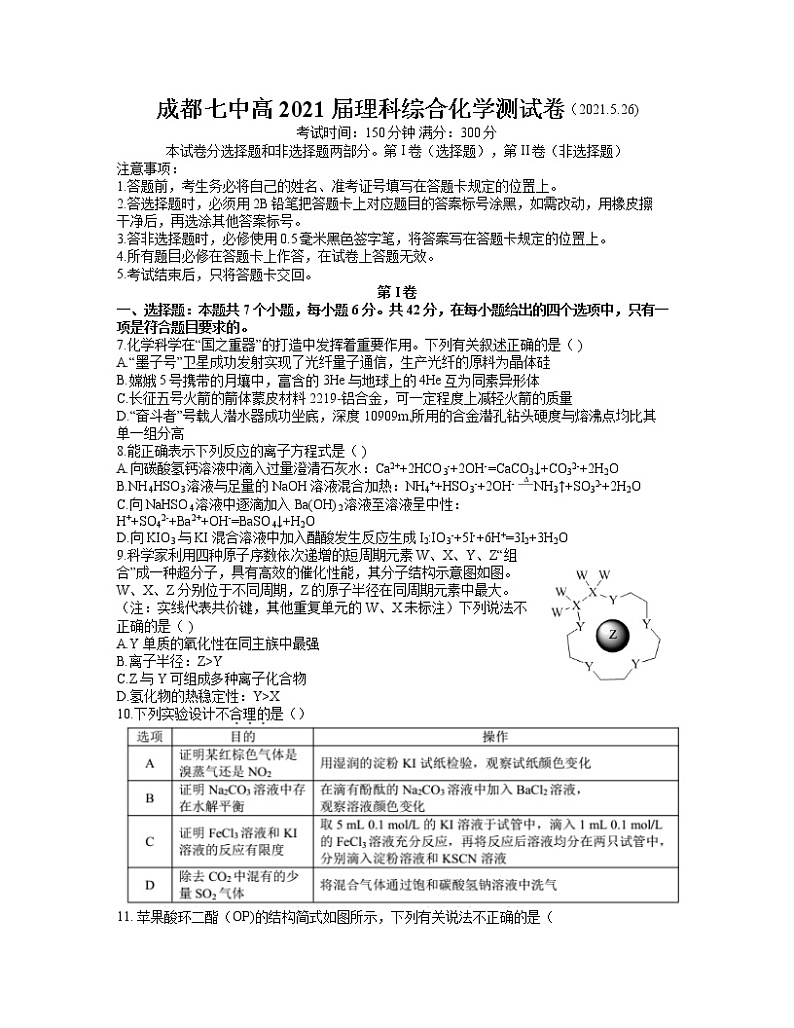
9.科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其分子结构示意图如图。W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。(注:实线代表共价键,其他重复单元的W、X未标注)下列说法不正确的是( )
A.Y单质的氧化性在同主族中最强
B.离子半径:Z>Y
C.Z与Y可组成多种离子化合物
D.氢化物的热稳定性:Y>X
10.下列实验设计不合理的是()
11. 苹果酸环二酯(OP)的结构简式如图所示,下列有关说法不正确的是(
A.OP中含有的官能团是羧基、酯基
B.OP 在酸性条件下水解的有机产物有两种
C.OP能与新制氢氧化铜悬浊液反应
D.1 ml OP 与Na2CO3溶液反应,最多消耗2ml Na2CO3
12.采用(NH4)2SO4和NH3·H2O混合溶液作为电解液,平行放置的两块不锈钢板分别作为阴极和阳极,将废铅膏(主要成分为PbO2)平铺在阴极板上,可得到铅单质。这是一种成本较低
的铅回收工艺,如下示意图:
下列说法错误的是( )
A.阴极板的电极阴极导杆、
PbO2+4e-+2H2O+4NH4+=Pb+4NH3·H2O
B.电子由阳极板沿阳极导杆移向外接电源正极
C.电解过程中,OH-向阴极板迁移
D.标准状况下,外电路中每转移4ml电子,阳极板产生22.4LO2
13.甲胺(CH3NH2)的性质与氨相似,25℃时向10 mL 0.1 ml·L-1的甲胺中逐滴滴入0.1ml·L-1稀盐酸。溶液中水电离出的氢离子浓度的负对数[用pC表示,pC=-1gc水 (H+)]与加入盐酸体积的关系如图所示。下列叙述错误的是( )
A.Kb(CH3NH2)的数量级为10-4
B.甲胺的电离方程式:
C.b点溶液的pH<7
D.e点溶液:
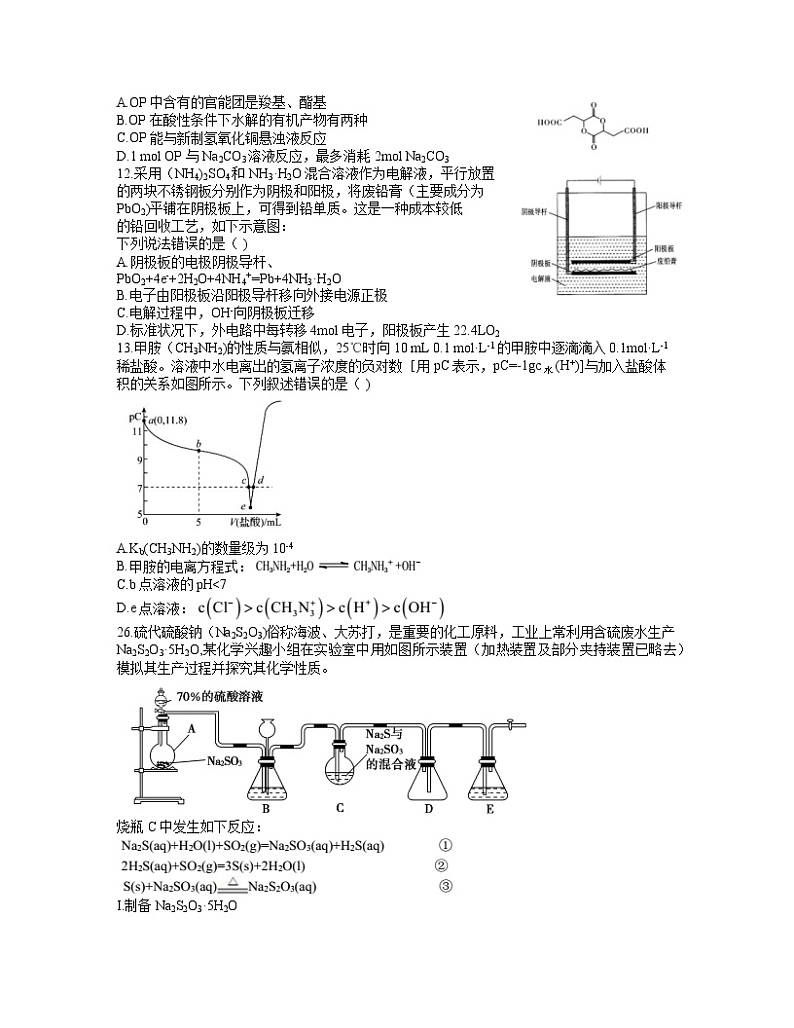
26.硫代硫酸钠(Na2S2O3)俗称海波、大苏打,是重要的化工原料,工业上常利用含硫废水生产Na2S2O3·5H2O,某化学兴趣小组在实验室中用如图所示装置(加热装置及部分夹持装置已略去)模拟其生产过程并探究其化学性质。
烧瓶C中发生如下反应:
I.制备Na2S2O3·5H2O
(1)加入药品之前须进行的操作是;装置D的作用是 ;装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用 (填字母)。
A. 蒸馏水B.饱和Na2SO3溶液C.饱和NaHSO3溶液D.饱和NaHCO3溶液
(2)为保证硫代硫酸钠的产量,实验中产生的SO2不能过量,原因是 ;该实验不使用
过浓或过稀的硫酸,而使用70%的硫酸的原因是 .
II.测定产品纯度
准确称取wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.10ml-L-1I2的标准溶液滴定。
反应原理为.
(3)滴定至终点时的现象: 。滴定起始和终点时I2的标准溶液液面位置如图所示,则消耗I2的标准溶液的体积为 mL.产品的纯度为 %(设Na2S2O3·5H2O的相对分子质量为M,列出用M、w表示的表达式)。
III.探究Na2S2O3的部分化学性质
(4)
实验结论: 。
IV.Na2S2O3的应用
(5)S2O32-可与一些金属离子形成稳定的络离子,常用于除重金属离子和照相行业的定影剂。已知AgBr 可溶于Na2S2O3溶液,生成配位数为2的络合物,请写出该化学方程式: .
27.三氧化二锑(Sb2O3)被称为锑白,不溶于水,溶于氢氧化钠溶液和酸,是应用最早的阻燃
剂。一种以辉锑矿(主要成分为Sb2S3,还含有Fe2O3、CuO、SiO2等)为原料制备锑白的工艺
流程如图所示:
已知:浸出液中含Sb5+、Sb3+、Fe3+、Cu2+.
回答下列问题:
(1)Sb在元素周期表中的位置为: .
(2)滤渣1的主要成分的化学式为 .。
(3)SbCl5可替代HCl(aq)和Cl2,写出SbCl5与Sb2S3反应的化学方程式: .。
(4)SbCl3分子中所有原子最外层均达到8e稳定结构,SbCl3的电子式为 .,
写出SbCl3水解的化学方程式: .。
(5)加入碱性物质中和时选用NH3·H2O而不选用NaOH溶液的原因是 .。
(6)电解SbCl3溶液时两极均为Sb3+放电,则生成Sb单质的为 .(填“阴”或“阳”)极;
写出另一极的电极反应式: .。
28.CO2的综合利用是当前研究的热点问题。2020年12月24日,中国科学院大气物理研究所
碳中和研究中心(筹)在北京挂牌成立。
回答下列问题:
(1)已知:I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·ml-l;
II.2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6 kJ·ml-l;
III.C(s)+2H2(g)=CH4(g) ΔH3=-74.8kJ·ml-1.
利用光能和光催化剂,将CO2(g)和H2O(g)转化为CH4(g)和O2(g)的热化学方程式为 .。
(2)一定温度下,将1mlCH4(g)和3mlCO2(g)充入起始压强为4MPa、体积为10L的恒容密闭容器中,一定条件下发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247 kJ·ml-1.
①下列事实可以判定反应达到平衡状态的是 (填选项字母)。
A. 为定值
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
②若上述反应10min末达到平衡,容器内的压强变为起始压强的1.25倍,则0~10min内,用CO2的浓度变化表示的平均反应速率v(CO2)= ;CH4的平衡转化率为 ;该反应的平衡常数Kp= MPa2(用平衡分压代替平衡浓度表示的平衡常数,分压=总压x该物质的物质的量分数)。
(3)一定条件下,CO2催化加氢可以合成乙醇:2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g).向I、II、III三个容积均为1L的恒容密闭容器中均充入1ml CO2(g)和3mlH2(g),在不同温度下发生上述反应。反应5min,测得各容器内CO2的物质的量如图所示:
①该反应的ΔH 0(填“>”或“<”)。
②5min后,向容器III中再充入1ml CO2(g)和1mlH2O(g),此时v逆 v正(填“>”“<”或“=”)。
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。通过人工光合作用制备
HCOOH的原理示意图如图所示:
催化剂a表面发生 (填“氧化”或“还原”)反应;催化剂b表面的电极反应式为 。
35.[化学-选修3:物质结构与性质](14分)
5月15日,天问一号探测器成功着陆于火星。据了解火星上存在大量的含氮化合物,科学家
推测火星生命可能主要以氮、碳、硅、铜为基体构成。
请回答下列问题:
(1)邻氨基吡啶()的铜配合物在有机不对称合成中起催化诱导效应。
①邻氨基吡啶中所有元素的电负性出小到大的顺序为 (填元素符号)。设NA为阿伏加德罗常数的值,1ml中含有σ键的数目为 。
②一定条件下-NH2可以被氧化成-NO2,-NO2中N原子的杂化方式为 杂化。
(2)第四周期的某主族元素,其第一至第五电离能数据如图所示,则该元素的基态原子电子排布式为 。
(3)元素周期表中的第IVA族~第VIIA族中部分元素的最简单氢化物的沸点变化趋势线如图,其中一个小黑点代表一种氢化物,则趋势线a代表第 族元素的最简单氢化物的沸点变化趋
势,判断依据是 。
(4)一种嘌呤和一种吡啶的结构如图。
①嘌呤中轨道之间的夹角∠1比∠2大,原因是 。
②分子中的大π键可以用符号表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡啶中的大π键可表示为 。
(5)火星岩石中存在大量的氮化镓,氮化镓为六方晶胞,结构如图所示。若该晶体密度为dgcm-3,晶胞参数a=b≠c(单位:nm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c
= nm(写出代数式)。
36.[化学-选修5:有机化学基础](14分)
盐酸罂粟碱(I)是一种非常有用的抗痉挛药物,用于治疗脑、心及其外周围血管痉挛所导致的缺血,肾、胆或者胃肠道等内脏的痉挛。我国科研工作者合成盐酸罂粟碱(1)的路线如图所示。
已知:Me为甲基;Et为乙基。
回答下列问题:
(1) 也可作为合成盐酸器粟碱(1)的原料,其名称为 ;E中无氧官能团的名称为 。
(2)B→C的反应类型为 。
(3)1mlH与氢气加成最多消耗 ml氢气,1个产物分子中有 个手性碳原子。
(4)写出D+E→F的化学方程式: 。
(5)M与C互为同分异构体,请写出满足下列条件的M有 种。
①含两个环,其中一个为苯环,两个环没有共用的碳原子
②硝基(-NO2)连在苯环上
核磁共振氢谱峰面积之比为4:2:2:2:1的结构简式: (任写一种)。
(6)请结合以上合成路线,写出以苯和上述流程中出现的物质为原料,合成的路线: 。
2022-2023学年四川省成都市龙泉中学蓉城名校联盟高三上学期第一次联考(月考)理综化学含解析: 这是一份2022-2023学年四川省成都市龙泉中学蓉城名校联盟高三上学期第一次联考(月考)理综化学含解析,共11页。试卷主要包含了4 × 10−7,K2 = 4,45%,4 kJ·ml−1等内容,欢迎下载使用。
四川省成都市石室天府中学2022届高三联测卷(四)理综化学试题含解析: 这是一份四川省成都市石室天府中学2022届高三联测卷(四)理综化学试题含解析,共23页。试卷主要包含了考生必须保证答题卡的整洁等内容,欢迎下载使用。
四川省成都市石室天府中学2022届高三联测卷(四)理综化学试题(解析版): 这是一份四川省成都市石室天府中学2022届高三联测卷(四)理综化学试题(解析版),共19页。试卷主要包含了考生必须保证答题卡的整洁等内容,欢迎下载使用。












